Содержание
Диагностика гликозилированного гемоглобина (HbA1c) в диагностическом центре им. Вытнова Д.И.
Сахарный диабет (СД), без преувеличения, продолжает играть одну из самых драматических ролей в истории мировой медицины.
Своевременная диагностика сахарного диабета позволяет провести профилактику, предупреждение развития СД и его осложнений.
Одним из методов диагностики является определение уровня глюкозы в крови. Поскольку измеренный уровень глюкозы показывает концентрацию на момент взятия крови, то сделать выводы о состоянии углеводного обмена в промежутках между измерениями сложно.
Показателем, который может дать усредненный уровень глюкозы в крови в течении длительного времени является гликозилированный гемоглобин (HbA1c).
Гликозилированный гемоглобин (употребляется также термин «гликированный гемоглобин») образуется в результате неферментативного присоединения глюкозы к N-концевым участкам R-цепей глобина гемоглобина А1 и обозначается как HbA1c. Концентрация HbA1c прямо пропорциональна средней концентрации глюкозы в крови. У здоровых концентрация HbA1c в крови от 4 до 6 %, у больных сахарным диабетом его уровень в 2-3 раза выше (в зависимости от степени гипергликемии). Образовавшийся HbA1c аккумулируется внутри эритроцитов и сохраняется в течение всего срока жизни эритроцита. Полупериод циркуляции эритроцита в кровяном русле составляет 60 суток, таким образом, концентрация HbA1c отражает уровень гликемии пациента за 60-90 дней до исследования [5, 6]. Огромное число исследований с использованием традиционных методов измерения содержания глюкозы подтвердило взаимосвязь HbA1c и уровня гликемии пациента. Результаты исследований, проведенных ГССТ в 90-х годах прошлого века, послужили основанием для подтверждения гипотезы о том, что уровень HbA1c отражает уровень глюкозы в крови и является эффективным критерием при мониторинге больных сахарным диабетом.
Концентрация HbA1c прямо пропорциональна средней концентрации глюкозы в крови. У здоровых концентрация HbA1c в крови от 4 до 6 %, у больных сахарным диабетом его уровень в 2-3 раза выше (в зависимости от степени гипергликемии). Образовавшийся HbA1c аккумулируется внутри эритроцитов и сохраняется в течение всего срока жизни эритроцита. Полупериод циркуляции эритроцита в кровяном русле составляет 60 суток, таким образом, концентрация HbA1c отражает уровень гликемии пациента за 60-90 дней до исследования [5, 6]. Огромное число исследований с использованием традиционных методов измерения содержания глюкозы подтвердило взаимосвязь HbA1c и уровня гликемии пациента. Результаты исследований, проведенных ГССТ в 90-х годах прошлого века, послужили основанием для подтверждения гипотезы о том, что уровень HbA1c отражает уровень глюкозы в крови и является эффективным критерием при мониторинге больных сахарным диабетом.
Уровень HbA1c признан золотым стандартом в оценке гликемического статуса пациентов с диабетом.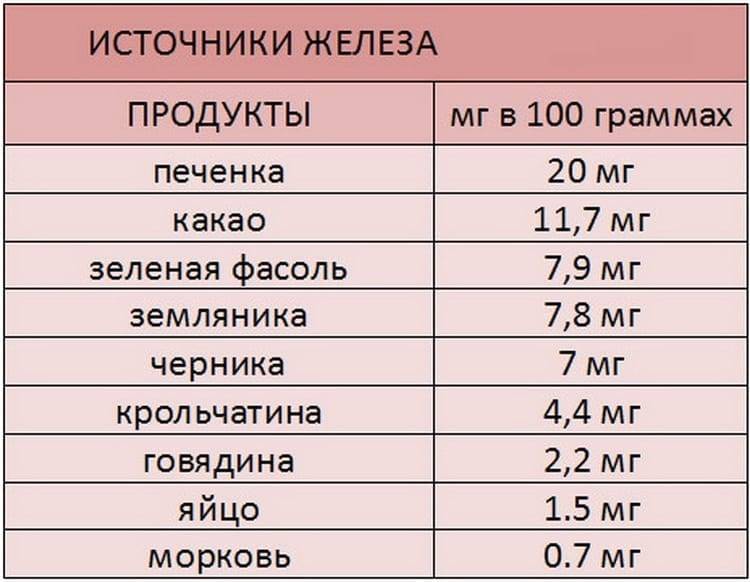
Многочисленные проспективные и эпидемиологические исследования указывают на улучшение гликемического контроля, оцененного по уровню HbA1c.
По многочисленным исследованиям гликированный гемоглобин доказал свою достоверность, продемонстрировав корреляцию со средними значениями гликемии, и отражает среднюю концентрацию глюкозы крови за предшествующие 2-3 месяца.
Исследования, выполняемые в лабораториях и по месту лечения, являются точными и правильными, если их соответствующим образом контролируют и адаптируют к международным стандартам.
Полагают, что случайное определение уровня глюкозы в плазме крови в клинических условиях не играет особой роли для качественного лечения больных СД.
В настоящее время все диабетические ассоциации используют понятие целевых значений гликированного гемоглобина. Так, последнее целевое значение HbA1c, рекомендуемое в Согласованном алгоритме ADA/ЕАSD на основании практичности и снижения развития осложнений, «в общей популяции <7%», с оговоркой «для конкретных пациентов HbA1c следует, насколько это возможно, приблизить к нормальному (<6%) без значимых гипогликемий».
Cоответствия уровня HbA1c среднесуточному уровню глюкозы в плазме в течение трех месяцев
| HbA1c, % | Глюкоза, ммоль/л | HbA1c, % | Глюкоза, ммоль/л | HbA1c, % | Глюкоза, ммоль/л |
| 4 | 3,8 | 9,5 | 12,5 | 15 | 21,3 |
| 4,5 | 4,6 | 10 | 13,3 | 15,5 | 22,1 |
| 5 | 5,4 | 10,5 | 14,1 | 16 | 22,9 |
| 5,5 | 6,2 | 11 | 14,9 | 16,5 | 23,7 |
| 6 | 7,0 | 11,5 | 15,7 | 17 | 24,5 |
| 6,5 | 7,8 | 12 | 16,5 | 17,5 | 25,3 |
| 7 | 8,6 | 12,5 | 17,3 | 18 | 26,1 |
| 7,5 | 9,4 | 13 | 18,1 | 18,5 | 26,9 | 8 | 10,2 | 13,5 | 18,9 | 19 | 27,7 |
| 8,5 | 11,0 | 14 | 19,7 | 19,5 | 28,5 |
| 9 | 11,7 | 14,5 | 20,5 | 20 | 29,2 |
Лаборатория «ДиаЛаб» рада сообщить Вам, что с недавних пор данное исследование выполняется на высококачественном анализаторе D10 (Bio Rad) с референсным методом высокоэффективной жидкостной хроматографии, который является золотым стандартом в количественном определении гликозилированного гемоглобина.
Правила взятия материала:
Перед взятием крови на данный анализ достаточно не употреблять пищу в течение двух часов.
Взятие крови осуществляют в пробирку с ЭДТА (сиреневая крышка).
Сразу же после взятия крови, не встряхивая, перевернуть пробирку 6-8 раз (пробирка перевернута правильно, если воздушный пузырек переместился из одного конца пробирки в другой). Резкое смешивание может вызвать пенообразование и гемолиз (агглютинация тромбоцитов).
Температура хранения: от 2 до 8 °С.
Срок выполнения: 1 рабочий день.
Гемоглобин у женщин ? норма, повышенный и низкий гемоглобин.
Без кислорода человек может прожить очень мало, а его нехватка существенным образом сказывается на здоровье и состоянии человеческого организма. Поэтому одним из важнейших элементов нашего организма является гемоглобин. Именно он выполняет столь необходимую для нас функцию – доставляет кислород ко всем тканям и клеткам.
Нормы
Гемоглобин представляет собой сложный белок, в состав которого входит железо. Особенностью данного белка является то, что он способен обратимо связываться с кислородом, разнося его ко всем клеткам организма.
Особенностью данного белка является то, что он способен обратимо связываться с кислородом, разнося его ко всем клеткам организма.
Помимо того, что гемоглобин способен связываться в легких с молекулами кислорода, он также может связываться с молекулами углекислого газа, которые вырабатываются в клетках нашего организма. Таким образом, он доставляет необходимый кислород и забирает ненужный углекислый газ.
Содержится гемоглобин в кровяных эритроцитах. Нужно сказать, что именно он обеспечивает ярко-красный цвет нашей крови. А точнее, содержащееся в нем железо.
Уровень содержания гемоглобина в крови, который принято считать нормой для взрослого человека, составляет:
- для мужчин – от 130 до 160 г/л;
- для женщин – от 120 до 150 г/л.
У детей нормальный уровень содержания гемоглобина в крови зависит от возраста. Так, к примеру, у новорожденных детей это значение является максимальным за всю человеческую жизнь – от 145 до 225 г/л.
Позднее, приблизительно к 6 месяцам, этот уровень снижается до минимального значения – от 95 до 135 г/л. И до 18 лет наблюдается относительно стабильное постепенное увеличение данного показателя.
Прочитать про нормы мочевой кислоты в крови можно в этой статье.
Снижение уровня гемоглобина в крови проявляется в следующих симптомах:
- бледность;
- сухость кожи;
- болезненный вид;
- повышенная утомляемость;
- приступы головокружения;
- постоянно холодные ладони и ступни.
Подобное отклонение от нормы врачи называют анемией (или же малокровием). Особенно внимательно нужно следить за уровнем гемоглобина детям и беременным женщинам.
Для детей пониженный уровень гемоглобина опасен тем, что недостаточное снабжение тканей кислородом может привести к серьезным последствиям, таким как задержка в росте и умственном развитии. Кроме того, дети становятся гораздо более восприимчивы к инфекционным заболеваниям.
У беременных женщин уровень гемоглобина может упасть из-за гормональной перестройки организма. А также вследствие того, что большую часть материнского гемоглобина забирает на себя ребенок.
Причиной пониженного уровня гемоглобина могут быть различного рода заболевания, которые не дают железу нормально усваиваться в организме. Большие кровопотери и перенесенные операции также вызывают снижение уровня гемоглобина.
Но основной причиной снижения данного показателя в наши дни выступает неправильное питание, которое не позволяет организму получать необходимое количество железа и микроэлементов, способствующих его усвоению в организме.
Пониженный уровень гемоглобина также очень часто встречается у тех, кто слишком изнуряет свой организм диетами и находится все время «в режиме похудения». В этом случае организм не может получить всех необходимых для него веществ, как бы ни старался худеющий сбалансировано питаться.
Как повысить?
Для повышения уровня гемоглобина в организме необходимо ввести в свой рацион продукты, которые отличаются высоким содержанием железа.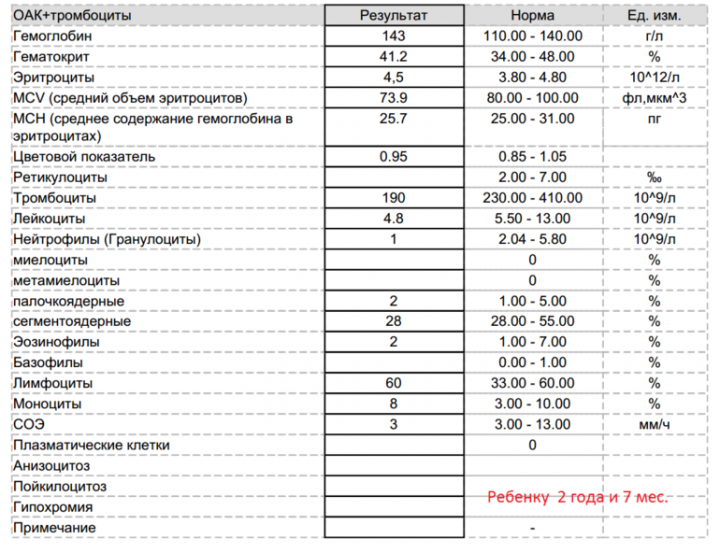 К таким продуктам относятся:
К таким продуктам относятся:
- мясо нежирных сортов;
- говяжья печень;
- различные каши, в особенности гречневая;
- любые свежевыжатые соки, в особенности гранатовый;
- яйца и молочные продукты.
Тем, кто страдает от пониженного уровня гемоглобина, настоятельно рекомендуют пить как можно меньше чая и кофе. Объясняется это тем, что эти напитки способствуют вымыванию из организма многих полезных веществ, в том числе и железа.
При медикаментозном повышении гемоглобина следует быть осторожным. Поскольку большинство препаратов, которые назначаются больным анемией, вызывают неприятные побочные эффекты со стороны ЖКТ, такие как диарея, запоры, тошнота или изжога.
Следует также отметить, что при очень низком уровне гемоглобина железоповышающая диета может быть только дополнением к медикаментозному лечению, которое пропишет вам лечащий врач. Полагаться исключительно на чудодейственные свойства продуктов питания в данном случае не стоит. Особенно, если речь идет о детях или беременных женщинах.
Особенно, если речь идет о детях или беременных женщинах.
Повышенный уровень гемоглобина и его причины
На повышение уровня гемоглобина в крови могут повлиять многие факторы, в том числе и место пребывания человека. Данный фактор особенно сказывается на тех, кто проживает в высокогорных районах. Ведь в горах воздух более разряжен и менее насыщен кислородом. Следовательно, повышение уровня гемоглобина является своеобразной компенсацией нехватки кислорода.
Кстати, у курящих людей может возникнуть похожая проблема. Но, если для жителей высокогорных районов высокий уровень гемоглобина – это своеобразная норма, то для курящих людей это выступает причиной серьезных неприятностей.
Повышенный гемоглобин может стать нормой для людей, которые профессионально занимаются спортом. То есть вследствие постоянных нагрузок, которым они подвергают свой организм, уровень гемоглобина имеет свойство повышаться.
Неправильное питание также может быть причиной повышения данного показателя.
Особенно, если в организме не хватает фолиевой кислоты и витамина В12.
Важно также помнить о существовании так называемого ложно повышенного гемоглобина. Подобное явление наблюдается при обезвоживании организма. За счет недостатка воды уменьшается объем плазмы крови. А, следовательно, повышается концентрация красных кровяных телец.
Симптомы повышенного содержания гемоглобина в крови могут быть во многом схожими с анемией. Те же самые приступы головокружения, повышенная утомляемость, бледность и болезненность. Однако в случае с повышением к перечисленным признакам добавляются еще и проблемы с органами мочеполовой системы.
Опасность высокого уровня гемоглобина в том, что кровь становится густой и вязкой. А это дает большую нагрузку на сердце, потому как нужно больше усилий, чтобы протолкать ее по сосудам. А также за счет густоты и вязкости в кровеносных сосудах могут образовываться тромбы. Они, в свою очередь, приводят к инфаркту или инсульту.
Также причиной повышения данного параметра могут быть нарушения в работе дыхательных путей или сердечно-сосудистой системы либо развитие онкологического заболевания.
Кроме всего прочего, у людей с повышенным уровнем гемоглобина в крови очень часто диагностируют сахарный диабет. Причиной тому может стать переизбыток глюкозы в крови. Стоит об этом задуматься, прежде чем заниматься самолечением и прописывать самому себе диеты.
Как понизить?
Для того, чтобы уровень гемоглобина в крови стал ниже, специалисты советуют следующее:
- пейте больше воды. Если уровень гемоглобина поднялся вследствие обезвоживания, то при восстановлении водного баланса все должно вернуться в норму;
- в отличие от случаев с пониженным гемоглобином, чай при повышении данного показателя абсолютно не воспрещается;
- сократить потребление красного мяса и субпродуктов, содержащих большое количество железа;
- употреблять как можно меньше рыбы и морепродуктов.
 Особенно это касается красных сортов рыбы, а также вяленой рыбы и морепродуктов. Поэтому любители сушеной рыбки или кальмаров должны умерить свою страсть к подобным продуктам;
Особенно это касается красных сортов рыбы, а также вяленой рыбы и морепродуктов. Поэтому любители сушеной рыбки или кальмаров должны умерить свою страсть к подобным продуктам; - основу вашего рациона должны составлять каши. Они хороши как для повышения уровня гемоглобина, так и для его понижения;
- употреблять больше растительных белков. Они содержатся в сое и бобовых;
- употреблять больше овощей (даже термически обработанных) и фруктов;
- исключить из рациона соки и газированные напитки. Соки содержат большое количество железа, а газированные напитки насыщены углекислым газом. А как уже было сказано выше, переизбыток углекислого газа (он же, по сути, и нехватка кислорода) – это прямой сигнал к повышению уровня гемоглобина;
- постараться не употреблять сахар и сладости. Эти продукты способствуют усвоению железа, а, следовательно, и увеличению его концентрации в организме;
- перестать употреблять алкоголь. Потому как этиловый спирт, соединяясь с железом, образует вещества, которые пагубно влияют на печень.
 А продукты распада алкоголя стимулируют выработку крови. Поэтому врачи заметили, что у регулярно выпивающих людей уровень гемоглобина, как правило, повышен;
А продукты распада алкоголя стимулируют выработку крови. Поэтому врачи заметили, что у регулярно выпивающих людей уровень гемоглобина, как правило, повышен; - постараться не употреблять красные ягоды, овощи и фрукты. Потому как они содержат большое количество веществ, вызывающих повышение уровня гемоглобина в крови.
В качестве заключения можно сказать, что низкий уровень гемоглобина, как и высокий, несет для человека определенную опасность. Собственно, как и любое отклонение от нормы. Прежде чем начинать заниматься самолечением и пытаться повысить или понизить гемоглобин собственным силами, следует пройти соответствующее обследование. Ведь отклонение данного показателя от нормы, особенно в сторону повышения, может быть последствием определенных заболеваний внутренних органов.
Обязательно следует обратиться за консультацией к вашему лечащему врачу. Именно он сможет квалифицированно и точно определить, что именно является причиной данной патологии конкретно в вашем случае.
Ведь за не очень серьезным, на первый взгляд, отклонением в организме могут скрываться куда более серьезные проблемы.
А высокий или низкий уровень гемоглобина просто выполняет функцию своеобразной «лакмусовой бумажки», индикатора неполадок в нашем организме.
Относитесь с должным вниманием к своему здоровью и здоровью ваших родных и близких!
Причины отклонений от нормы гемоглобина у женщин
Нормальные показатели гемоглобина у женщин отличаются по возрастным периодам. Любые отклонения в большую или меньшую сторону могут указывать на различные нарушения. Поэтому нужно постоянно контролировать уровень гемоглобина, чтобы вовремя обнаруживать возможные заболевания.
Гемоглобин – это пигмент, содержащий железо и окрашивающий кровь в красный цвет. Он необходим для транспортировки кислорода к тканям, а изменение его уровня указывает на нарушение этой функции. В результате могут развиться различные болезни – анемия, гипоксемия и другие.
Гемоглобин содержится в эритроцитах
Для определения уровня гемоглобина проводится общий анализ крови из пальца. Проводить анализ необходимо натощак, не принимать пищу минимум 8 часов до него. Во время анализа определяются число эритроцитов и присутствие аномальных клеток в исследуемом материале.
Нормальный уровень гемоглобина отличается по возрасту.
- У женщин младше 30 он составляет 112–150 г/л. В этот период его уровень может достигнуть максимальных значений. А после перехода этого рубежа уровень показателей начинает постепенно снижаться. Для женщин от 30 до 40 лет являются нормальными значения 120–145 г/л.
- В период между 40 и 50 годами гемоглобин снижается еще примерно на 5 г/л, и нормальными значениями являются 120–140 г/л. Состав крови заметно изменяется к концу этого периода из-за гормональной перестройки.
- После пересечения рубежа в 50 лет нормальными являются показатели 115–138 г/л. Но гемоглобин может быть еще более низким из-за нестабильности гормонального фона, что характерно для периода менопаузы.
 На состав крови могут повлиять также высокая эмоциональность и слабая стрессоустойчивость.
На состав крови могут повлиять также высокая эмоциональность и слабая стрессоустойчивость. - После 60 лет: к этому времени должен завершиться период климакса, обменные процессы замедляются. Потребность в питательных компонентах уменьшается, поэтому железо хуже усваивается организмом. Для женщин старше 60 лет нормальные значения гемоглобина составляют 105–130 г/л.
Во время месячных и при беременности эти значения могут немного отклоняться в сторону.
Во время вынашивания плода в организме женщины накапливается жидкость, что приводит к физиологическому разбавлению крови. Для беременных нормальные значения составляют 110–155 г/л.
Чрезмерное снижение показателей может быть связано с недостатком железа и витамина B9. Эти вещества используются плодом во время развития, поэтому постепенно может возникнуть их нехватка в женском организме. Очень низкий гемоглобин может привести к тому, что возникнет гипоксия плода.
Во время менструации происходит кровопотеря, после чего объем ее восстанавливается, но медленно.
Поэтому для такого периода является нормальным снижение гемоглобина. Если месячные необильные, мажущие, это может свидетельствовать об увеличенном уровне железа и большой вязкости крови.
Низкие показатели гемоглобина могут свидетельствовать об анемии. Это состояние может быть связано с рядом факторов.
- Неправильное питание, из-за чего в организм человека попадает недостаточное количество витаминов группы B и железа. Такая проблема может наблюдаться у вегетарианцев, поскольку железо из животных продуктов усваивается лучше, чем из растительных.
- Наличие паразитов в кишечнике. Они могут перехватывать поступающие компоненты и использовать их в процессе своей жизнедеятельности. А в организме хозяина развивается дефицит веществ.
- Серьезные кровотечения – желудочные, послеоперационные, менструальные, послеродовые.
- Донорство крови с несоблюдением правил проведения процесса, взятие чрезмерного объема крови.
- Наследственные патологии, инфекционные и аутоиммунные болезни.

- Рак поджелудочной железы, из-за чего в организм выбрасывается чрезмерное количество инсулина.
- Гепатиты всех типов.
- Злоупотребление лекарственными препаратами и другие факторы.
Анемию нужно срочно лечить, иначе она может вызвать серьезные проблемы со здоровьем. Для профилактики ее развития необходимо следить за своим питанием. В рацион обязательно включить продукты, содержащие гемовое железо, синтезирующее гемоглобин. Это красное мясо, морепродукты и другие.
Уровень гемоглобина определяется с помощью общего анализа крови
Повышенный гемоглобин не менее опасен. Он может привести к проблемам с мочеиспусканием, ухудшению зрения, потере аппетита, увеличению печени и к прочим осложнениям.
Причин такого явления может быть несколько:
- некоторые заболевания – эритроцитоз, болезни сердца, дыхательной системы и прочие патологии;
- незначительное повышение показателей может быть связано с переливанием крови;
- проживание в горной местности или работа на большой высоте часто являются причиной высоких показателей гемоглобина, которые являются для человека нормальными;
- длительный прием мочегонных лекарств, обезвоживание организма;
- курение – при вдыхании сигаретного дыма в легкие поступает недостаточное количество кислорода.
 Организм может отреагировать на это повышением гемоглобина;
Организм может отреагировать на это повышением гемоглобина; - ожоги, из-за которых разрушаются эритроциты, и из них выделяется гемоглобин. Высокие его значения могут наблюдаться при обширных ожогах.
Гликированный гемоглобин, показывающий содержание сахара в организме за последние 3–4 месяца, может повыситься при сахарном диабете. Такой показатель отражает процентное содержание гемоглобина, соединенного с молекулами глюкозы. При сахарном диабете повышается уровень глюкозы, что ведет к увеличению содержания гликированного гемоглобина.
Чтобы определить, почему появились нарушения, необходимо пройти комплексное диагностическое обследование. Для постановки диагноза может потребоваться консультация у гастроэнтеролога, иммунолога, эндокринолога и других специалистов.
Отклонения от нормы в обе стороны сопровождаются похожими признаками:
- бессонница;
- побледнение кожных покровов, иногда формирование белых пятен на коже;
- сухость во рту, трещины на губах;
- нарушение сердечного ритма;
- сильные головные боли и мигрени;
- ломкие волосы, которые обильно опадают;
- слоящиеся ногти;
- иногда измененный гемоглобин у женщин приводит к изменению вкусовых ощущений.

При возникновении вышеперечисленной симптоматики необходимо незамедлительно обратиться к врачу. Чем быстрее обнаружить и вылечить проблему, тем меньше вероятность развития осложнений.
Терапия состояний, при которых наблюдается высокий или пониженный уровень гемоглобина в крови, отличается. Самостоятельно принимать какие-то препараты запрещено, иначе могут развиться серьезные осложнения.
При низком гемоглобине врач назначает железосодержащие препараты. Их дозировку он определяет в зависимости от уровня гемоглобина и от возраста пациентки. В среднем длительность лечения составляет около 2 недель.
Для снижения уровня гемоглобина назначаются препараты, предназначенные для разжижения крови. Т
Эффективность трансфузий донорских эритроцитов у больных гемобластозами с анемией
Н.А. Романенко, Р.А. Головченко, С.С. Бессмельцев, Н.А. Потихонова, А.В. Чечеткин, К.М. Абдулкадыров
ФГБУ «Российский научно-исследовательский институт гематологии и трансфузиологии Федерального медико биологического агентства России», г. Санкт-Петербург
Санкт-Петербург
Трансфузиология №2, 2015
Резюме
В статье представлен анализ результатов коррекции анемии с помощью трансфузий эритроцитов (ТЭ) у 190 пациентов с различными формами гемобластозов. Эффективность ТЭ определялась уменьшением клинической симптоматики анемии и приростом содержания гемоглобина на одну перелитую дозу эритроцитов. Полный ответ на ТЭ в виде прироста содержания гемоглобина на 10 г/л (11,4 ± 0,6 г/л) констатирован у 57 (30%) пациентов, концентрация Hb у которых увеличилась с 70,4 ± 1,7 до 103,4 ± 0,9 г/л после переливания 2,9 ± 0,2 доз эритроцитов. Общая выживаемость (ОВ) за период 4 месяцев составила 94,7%. Частичный ответ на ТЭ в виде прироста содержания Hb на 5–9,9 г/л (6,6 ± 0,2 г/л) на каждую перелитую дозу эритроцитов констатирован у 71 (37,4%) пациента. У них уровень Hb увеличился с 68,7 ± 1,4 до 97,6 ± 1,2 г/л, перелито 4,5 ± 0,3 единицы эритроцитов. ОВ в течение 4 месяцев составила 84,5%. Минимальный ответ в виде прироста гемоглобина на каждую дозу эритроцитов на <5 г/л (2,6 ± 0,2 г/л) констатирован у 62 (32,6%) больных. У них концентрация Hb увеличилась с 72,5 ± 1,6 до 89,2 ± 1,8 г/л, перелито 6,4 ± 0,8 доз эритроцитов. ОВ в течение 4 месяцев составил 66,1%, что существенно ниже, чем в группах больных с полным и частичным ответом. Низкая эффективность ТЭ отмечалась у пациентов с тяжелой депрессией эритропоэза, гемолизом эритроцитов вследствие прогрессирования заболевания и токсического эффекта химиотерапии. Стратификация больных на группы в зависимости от эффективности ТЭ позволяет прогнозировать течение основного заболевания и дифференцированно подходить к терапии анемии при гемобластозах.
У них концентрация Hb увеличилась с 72,5 ± 1,6 до 89,2 ± 1,8 г/л, перелито 6,4 ± 0,8 доз эритроцитов. ОВ в течение 4 месяцев составил 66,1%, что существенно ниже, чем в группах больных с полным и частичным ответом. Низкая эффективность ТЭ отмечалась у пациентов с тяжелой депрессией эритропоэза, гемолизом эритроцитов вследствие прогрессирования заболевания и токсического эффекта химиотерапии. Стратификация больных на группы в зависимости от эффективности ТЭ позволяет прогнозировать течение основного заболевания и дифференцированно подходить к терапии анемии при гемобластозах.
Ключевые слова: анемия, эритроциты, трансфузии эритроцитов, содержание гемоглобина, гематокрит, гемобластозы, донорские эритроциты.
Введение
Анемический синдром при онкогематологических заболеваниях является частым проявлением болезни, ухудшает ее прогноз и качество жизни пациентов. Указанный синдром характеризуется многочисленной клинической симптоматикой, приводящей к дезадаптации пациента в эмоциональной, социальной, семейной сферах [1, 2]. Частота анемии варьирует в зависимости от варианта, а также фазы опухолевого процесса и колеблется от 20 до 90%, а в период проведения химиотерапии (ХТ) может возрастать в 1,5–2 раза [3–7].
Частота анемии варьирует в зависимости от варианта, а также фазы опухолевого процесса и колеблется от 20 до 90%, а в период проведения химиотерапии (ХТ) может возрастать в 1,5–2 раза [3–7].
Основным методом коррекции анемии у больных опухолевыми заболеваниями системы крови являются трансфузии эритроцитов (ТЭ), позволяющие обеспечить адекватное функционирование органов и систем организма и качество жизни больных. Однако переливания донорских компонентов крови нередко осложняются иммунными реакциями с гемолизом, трансмиссивными инфекциями, тромбозами сосудов, а многократные ТЭ могут приводить к гемосидерозу внутренних органов [8–12]. Поэтому в последние годы принята ограничительная тактика к использованию гемотрансфузий [13–15]. Правила переливаний донорских эритроцитов определены Приказами Минздрава РФ № 363 от 25 ноября 2002 года «Об утверждении Инструкции по применению компонентов крови» и № 183н от 2 апреля 2013 г. «Об утверждении правил клинического использования донорской крови и (или) ее компонентов» [14, 15]. Согласно указаниям нормативных документов, показанием к переливанию донорских эритроцитов при острой анемии вследствие массивной кровопотери является потеря 25–30% объема циркулирующей крови, сопровождающаяся снижением уровня гемоглобина ниже 70–80 г/л и гематокрита ниже 25%, а также возникновением циркуляторных нарушений. Пациентам с хронической анемией донорские эритроциты переливают по более строгим показаниям, что обусловлено компенсаторными механизмами организма реципиента (увеличение сердечного выброса, сдвиг кривой диссоциации оксигемоглобина вправо, увеличение отдачи кислорода в тканях). Этим больным переливают эритроциты только для коррекции важнейших симптомов, обусловленных анемией [15].
Согласно указаниям нормативных документов, показанием к переливанию донорских эритроцитов при острой анемии вследствие массивной кровопотери является потеря 25–30% объема циркулирующей крови, сопровождающаяся снижением уровня гемоглобина ниже 70–80 г/л и гематокрита ниже 25%, а также возникновением циркуляторных нарушений. Пациентам с хронической анемией донорские эритроциты переливают по более строгим показаниям, что обусловлено компенсаторными механизмами организма реципиента (увеличение сердечного выброса, сдвиг кривой диссоциации оксигемоглобина вправо, увеличение отдачи кислорода в тканях). Этим больным переливают эритроциты только для коррекции важнейших симптомов, обусловленных анемией [15].
Однако у пациентов с онкогематологическими заболеваниями в период проведения химиотерапии содержание гемоглобина в крови нередко снижается на 10–40 г/л, усугубляя имеющуюся анемию и функции жизненно важных органов и систем. Течение анемии также усугубляют гемолиз эритроцитов, гипоплазия костного мозга (КМ), интоксикация за счет распада опухолевых клеток [16]. Кроме того, хроническая анемия может нередко приводить к дистрофическим изменениям в миокарде с развитием сердечной недостаточности, что отражается в том числе на прогнозе заболевания и качестве жизни больного [2]. Поэтому таким пациентам необходимо обеспечить адекватную газотранспортную функцию крови, позволяющую избежать осложнений со стороны сердечно-сосудистой системы. Оптимальным ответом на каждую перелитую дозу донорских эритроцитов, содержащую 180–260 мл эритроцитов, принято считать увеличение в периферической крови содержания Hb на 10 г/л у пациента с массой тела 70–80 кг [16–18]. Однако у больных с дефектом эритропоэза, гипоплазией КМ, гемолизом эритроцитов не всегда удается достичь оптимального ответа, что ставит задачу по выявлению причин низкой эффективности ТЭ и влияние ее на общую выживаемость (ОВ) больных гемобластозами.
Кроме того, хроническая анемия может нередко приводить к дистрофическим изменениям в миокарде с развитием сердечной недостаточности, что отражается в том числе на прогнозе заболевания и качестве жизни больного [2]. Поэтому таким пациентам необходимо обеспечить адекватную газотранспортную функцию крови, позволяющую избежать осложнений со стороны сердечно-сосудистой системы. Оптимальным ответом на каждую перелитую дозу донорских эритроцитов, содержащую 180–260 мл эритроцитов, принято считать увеличение в периферической крови содержания Hb на 10 г/л у пациента с массой тела 70–80 кг [16–18]. Однако у больных с дефектом эритропоэза, гипоплазией КМ, гемолизом эритроцитов не всегда удается достичь оптимального ответа, что ставит задачу по выявлению причин низкой эффективности ТЭ и влияние ее на общую выживаемость (ОВ) больных гемобластозами.
Материалы и методы
Исследована эффективность ТЭ у 190 пациентов (в возрасте от 18 до 81 года) с гемобластозами, находившихся в гематологической клинике ФГБУ «РосНИИ ГТ» на лечении в период 2006–2013 гг. Среди исследуемых были 39 пациентов с миелодиспластическим синдромом (МДС), 28 – острым миелоидным лейкозом (ОМЛ), 21 – первичным миелофиброзом (ПМФ), 10 – хроническим миелолейкозом (ХМЛ) в фазе бластного криза, 42 – множественной миеломой (ММ) в III стадии, 19 – неходжкинскими лимфомами (НХЛ) в III–IV стадиях, 22 – хроническим лимфолейкозом (ХЛЛ) в стадии C (по J.L. Binet), 9 – острым лимфобластным лейкозом (ОЛЛ). В исследуемую группу входили молодые пациенты со стабильным статусом и больные по- жилого возраста (старше 65 лет) с наличием сопутствующей сердечной, легочной недостаточности, а также больные с нестабильным течением основного заболевания (сепсис, неустойчивые показатели периферической крови, геморрагический синдром, гемолиз). По степени тяжести анемии (по классификации ВОЗ) были выделены 3 группы больных: с умеренной анемией (n = 49), с выраженной анемией (n = 61) и с анемией угрожающей степени тяжести (n = 80).
Среди исследуемых были 39 пациентов с миелодиспластическим синдромом (МДС), 28 – острым миелоидным лейкозом (ОМЛ), 21 – первичным миелофиброзом (ПМФ), 10 – хроническим миелолейкозом (ХМЛ) в фазе бластного криза, 42 – множественной миеломой (ММ) в III стадии, 19 – неходжкинскими лимфомами (НХЛ) в III–IV стадиях, 22 – хроническим лимфолейкозом (ХЛЛ) в стадии C (по J.L. Binet), 9 – острым лимфобластным лейкозом (ОЛЛ). В исследуемую группу входили молодые пациенты со стабильным статусом и больные по- жилого возраста (старше 65 лет) с наличием сопутствующей сердечной, легочной недостаточности, а также больные с нестабильным течением основного заболевания (сепсис, неустойчивые показатели периферической крови, геморрагический синдром, гемолиз). По степени тяжести анемии (по классификации ВОЗ) были выделены 3 группы больных: с умеренной анемией (n = 49), с выраженной анемией (n = 61) и с анемией угрожающей степени тяжести (n = 80).
Переливания донорских эритроцитов и оценка их эффективности проводились в соответствии с «Инструкцией по применению компонентов крови» [15]: после каждой гемотрансфузии эритроцитов исследовали гемограмму, общий анализ мочи. Назначались ТЭ при наличии жалоб на выраженную слабость, сердцебиение, одышку при минимальной физической активности, резкое снижение работоспособности, тахикардию, а также при содержании
Назначались ТЭ при наличии жалоб на выраженную слабость, сердцебиение, одышку при минимальной физической активности, резкое снижение работоспособности, тахикардию, а также при содержании
гемоглобина <80 г/л, гематокрита <25%. Прекращали трансфузии эритроцитов при достижении содержания гемоглобина 85–95 г/л и выше. Показания расширяли (содержание гемоглобина <95 г/л и гематокрита <30%) у пациентов пожилого возраста с сердечной или легочной недостаточностью. Эффективность ТЭ оценивали по уменьшению клинической симптоматики анемии и приросту концентрации гемоглобина. В зависимости от прироста концентрации Hb на одну дозу перелитых донорских эритроцитов пациентов подразделили на три группы: с положительным (полным) ответом (прирост уровня Hb 10 г/л), частичным (на 5–9,9 г/л) и минимальным (на <5 г/л).
Для коррекции анемии назначали фильтрованную эритроцитную массу (ФЭМ), отмытые эритроциты (ОЭ), размороженные и отмытые эритроциты (РЭМ), а также эритроцитную массу (ЭМ). Учитывая, что часть пациентов получала многократные переливания донорских эритроцитов (в течение >2 мес.), им исследовали кровь на наличие алло- и аутоантиэритроцитарных антител и при наличии подозрения на возможную несовместимость (n = 16) ТЭ производили после индивидуального подбора донорских эритроцитов с учетом комплекса антигенов по системе Резус.
Учитывая, что часть пациентов получала многократные переливания донорских эритроцитов (в течение >2 мес.), им исследовали кровь на наличие алло- и аутоантиэритроцитарных антител и при наличии подозрения на возможную несовместимость (n = 16) ТЭ производили после индивидуального подбора донорских эритроцитов с учетом комплекса антигенов по системе Резус.
При коррекции анемии учитывались не только симптомы анемии, показатели гемограммы, но и генез развития анемии. Так, в ходе исследования выявлено, что основными причинами анемии были опухолевая инфильтрация КМ и уменьшение плацдарма эритроидного ростка (у 41 пациента число эритроидных предшественников в стернальном пунктате составляло от 0,2 до 9,8%), гемолиз эритроцитов (у 25 больных – повышение непрямой фракции билирубина от 19,2 до 41,9 мкмоль/л), иногда выявлялся дефицит железа (у 24 пациентов сывороточное железо составляло от 4,0 до 8,8 мкмоль/л), наблюдался геморрагический синдром (у 16 больных, включая желудочнокишечные и носовые кровотечения), обусловленный ДВС-синдромом или тромбоцитопенией. При наличии дефицита железа помимо ТЭ назначали препараты железа. Для остановки кровотечения применялись свежезамороженная плазма, концентрат тромбоцитов в терапевтических дозах в комплексе с гемостатическими препаратами.
При наличии дефицита железа помимо ТЭ назначали препараты железа. Для остановки кровотечения применялись свежезамороженная плазма, концентрат тромбоцитов в терапевтических дозах в комплексе с гемостатическими препаратами.
Статистическую обработку полученных результатов выполняли с использованием прикладных программ Microsoft Windows (Microsoft Excel, Ver. 2007) и STATISTICA 7.0 for Windows. Различия считали достоверными при p < 0,05.
Результаты исследования
В ходе проведенного анализа выявлено, что самой востребованной оказалась фильтрованная эритроцитная масса (табл. 1), которая применялась в 5,5 раза чаще по сравнению с ОЭ или РЭМ (p < 0,02) и в 15 раз чаще, чем ЭМ (p < 0,0001).
На фоне ТЭ у пациентов отмечалась положительная клиническая динамика – существенно уменьшилась симптоматика анемии и улучшились показатели периферической крови (табл. 2). При этом содержание гемоглобина в целом по группе увеличилось с 70,4 ± 0,9 до 98,6 ± 1,0 г/л (p < 0,001), а его прирост констатирован в среднем 28,9 ± 1,2 г/л, что соответствовало 8,0 ±0,4 г/л (1–30 г/л) из расчета на каждую перелитую дозу эритроцитов. Аналогично отмечалось и повышение количества эритроцитов в среднем на 0,92 ± 0,03×10¹²/л и уровня гематокрита в среднем на 8,3 ± 0,3%.
Аналогично отмечалось и повышение количества эритроцитов в среднем на 0,92 ± 0,03×10¹²/л и уровня гематокрита в среднем на 8,3 ± 0,3%.
При сравнительном анализе выявлено, что число доз эритроцитов в зависимости от возраста больных существенно не различалось; так, молодым пациентам (от 18 до 65 лет) и пациентам старшего возраста (от 66 до 81 года) для коррекции анемии потребовалось в среднем 5,1 ± 0,5 и 4,3 ± 0,4 дозы соответственно (p > 0,05).
Однако на фоне ТЭ не у всех пациентов одинаково повышались показатели периферической крови, что позволило разделить пациентов на группы в зависимости от увеличения уровня Hb на одно переливание эритроцитов (табл. 3).
Группа больных с полным ответом на ТЭ составила 30,0% (n = 57). Уровень Hb повышался на 10 г/л (в среднем на 11,4 ± 0,6 г/л) после каждого переливания эритроцитов, уменьшалась симптоматика анемии (одышка, слабость, головокружение, сердцебиение, гипотония, гиподинамия и т. д.). В данную группу вошли пациенты с онкогематологическими заболеваниями с благоприятным прогнозом по основному заболеванию и хорошо реагировавшие на противоопухолевую терапию. Этим больным переливались в среднем 2,9 ± 0,2 (1–7) дозы эритроцитов. В результате содержание гемоглобина увеличилось (рис. 1) с 70,4 ± 1,7 до 103,4 ± 0,9 г/л. Необходимо подчеркнуть, что у 41 пациента после трансфузий эритроцитов быстро выросли показатели эритрона (Hb >100 г/л, Ht >30%) не только благодаря высокой эффективности ТЭ, но и регенеративной активности КМ больных. В этой группе пациентов в течение четырех месяцев после ТЭ общая выживаемость составила 94,7%. Летальных исходов в этой группе констатировано 3 (5,3%) из 57 больных; при этом у 2 больных ММ развилась острая почечная недостаточность (1 пациентка с ММ III ст. В) и острая сердечная недостаточность (1 пациентка с ММ III ст. А), и у 1 – с ХЛЛ С стадией по J.L. Binet – развилась тяжелая двусторонняя пневмония.
Этим больным переливались в среднем 2,9 ± 0,2 (1–7) дозы эритроцитов. В результате содержание гемоглобина увеличилось (рис. 1) с 70,4 ± 1,7 до 103,4 ± 0,9 г/л. Необходимо подчеркнуть, что у 41 пациента после трансфузий эритроцитов быстро выросли показатели эритрона (Hb >100 г/л, Ht >30%) не только благодаря высокой эффективности ТЭ, но и регенеративной активности КМ больных. В этой группе пациентов в течение четырех месяцев после ТЭ общая выживаемость составила 94,7%. Летальных исходов в этой группе констатировано 3 (5,3%) из 57 больных; при этом у 2 больных ММ развилась острая почечная недостаточность (1 пациентка с ММ III ст. В) и острая сердечная недостаточность (1 пациентка с ММ III ст. А), и у 1 – с ХЛЛ С стадией по J.L. Binet – развилась тяжелая двусторонняя пневмония.
Группа пациентов с частичным ответом на ТЭ составила 37,4% (n = 71). У этих больных после каждого переливания эритроцитов отмечалось повышение содержания гемоглобина на 5,0–9,7 г/л (в среднем на 6,6 ± 0,2 г/л), уменьшение симптомов анемии, а при отмене переливаний через 10–15 дней наблюдалось умеренное снижение показателей эритрона, как правило, не требующее повторных трансфузий. В данную группу вошли преимущественно пациенты с благоприятным прогнозом (n = 47) и с рецидивами и рефрактерными формами заболевания: МДС (n = 8) – рефрактерная анемия с избытком бластов (РАИБ I и II), ОМЛ из предшествующего МДС (n = 5) и ОМЛ, вызванный предшествующим лечением (n = 3), ХМЛ бластный криз (n = 3), ММ, резистентная к химиотерапии (n = 4), синдром Рихтера при хроническом лимфолейкозе (n = 1). Этим больным переливались в среднем по 4,5 ± 0,3 (1–10) дозы эритроцитов. За время гемотрансфузий содержание гемоглобина повысилось с 68,7 ± 1,4 до 97,6 ± 1,2 г/л. ОВ в пределах 4 месяцев составила 84,5%. Летальные исходы больных (11 из 71, или 15,5%) были обусловлены рефрактерностью к проводимой противоопухолевой терапии и прогрессией основного заболевания.
В данную группу вошли преимущественно пациенты с благоприятным прогнозом (n = 47) и с рецидивами и рефрактерными формами заболевания: МДС (n = 8) – рефрактерная анемия с избытком бластов (РАИБ I и II), ОМЛ из предшествующего МДС (n = 5) и ОМЛ, вызванный предшествующим лечением (n = 3), ХМЛ бластный криз (n = 3), ММ, резистентная к химиотерапии (n = 4), синдром Рихтера при хроническом лимфолейкозе (n = 1). Этим больным переливались в среднем по 4,5 ± 0,3 (1–10) дозы эритроцитов. За время гемотрансфузий содержание гемоглобина повысилось с 68,7 ± 1,4 до 97,6 ± 1,2 г/л. ОВ в пределах 4 месяцев составила 84,5%. Летальные исходы больных (11 из 71, или 15,5%) были обусловлены рефрактерностью к проводимой противоопухолевой терапии и прогрессией основного заболевания.
Группа пациентов с минимальным ответом на переливания эритроцитов составила 32,6% (n = 62). Больные этой группы, как правило, нуждались через 10–14 дней в повторных гемотрансфузиях. Прирост гемоглобина после каждого переливания эритроцитов не превышал 4,9 г/л (в среднем 2,6 ± 0,2 г/л). Повышение концентрации гемоглобина отмечено с 72,5 ± 1,6 до 89,2 ± 1,8 г/л. Низкий прирост уровня Hb в этой группе, а в последующем и быстрое его снижение после ТЭ обусловлены преимущественно гемолизом (повышение общего билирубина 20,5 мкмоль/л – у 19 больных), выраженным угнетением кроветворения (снижение эритроидных элементов КМ менее 5% – у 17 пациентов) за счет рефрактерности заболевания к противоопухолевой терапии, а также токсическим эффектом ХТ (гематологическая токсичность III–IV ст.). Этим пациентам для улучшения состояния в последующем было перелито существенно большее количество доз донорских эритроцитов – в среднем 6,4 ± 0,8 (2–32), за счет чего удалось повысить уровень гемоглобина и гематокрит. В данную группу вошли пациенты с рефрактерными формами гемобластозов. ОВ в течение 4 месяцев составила 66,1%. Летальные исходы пациентов в течение четырех месяцев в этой группе больных (21 из 62 – 33,9%) были обусловлены рефрактерностью к ХТ и прогрессией основного заболевания.
Повышение концентрации гемоглобина отмечено с 72,5 ± 1,6 до 89,2 ± 1,8 г/л. Низкий прирост уровня Hb в этой группе, а в последующем и быстрое его снижение после ТЭ обусловлены преимущественно гемолизом (повышение общего билирубина 20,5 мкмоль/л – у 19 больных), выраженным угнетением кроветворения (снижение эритроидных элементов КМ менее 5% – у 17 пациентов) за счет рефрактерности заболевания к противоопухолевой терапии, а также токсическим эффектом ХТ (гематологическая токсичность III–IV ст.). Этим пациентам для улучшения состояния в последующем было перелито существенно большее количество доз донорских эритроцитов – в среднем 6,4 ± 0,8 (2–32), за счет чего удалось повысить уровень гемоглобина и гематокрит. В данную группу вошли пациенты с рефрактерными формами гемобластозов. ОВ в течение 4 месяцев составила 66,1%. Летальные исходы пациентов в течение четырех месяцев в этой группе больных (21 из 62 – 33,9%) были обусловлены рефрактерностью к ХТ и прогрессией основного заболевания.
В ходе сравнительного анализа выявлено, что прирост уровня гемоглобина существенно отличался, достигая соответственно 103,4 ± 0,9; 97,6 ± 1,2 г/л (p = 0,004) и 89,2 ± 1,8 г/л (p < 0,001), хотя исходные концентрации Hb были практически одинаковые (70,4 ± 1,7; 68,7 ± 1,4 г/л и 72,5 ± 1,6 г/л; p > 0,3).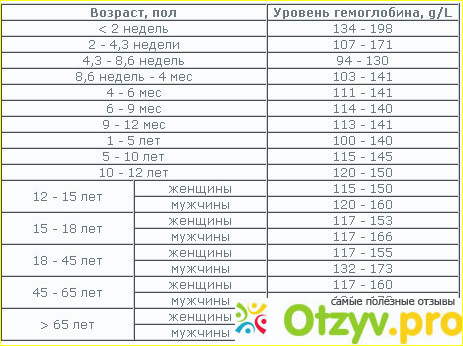 Значительно отличалась и общая выживаемость (рис. 2) в пределах 4 месяцев (с начала гемотрансфузий).
Значительно отличалась и общая выживаемость (рис. 2) в пределах 4 месяцев (с начала гемотрансфузий).
Так, если в 1-й группе общая выживаемость составила 94,7% (из 57 умерло 3 больных), во 2-й – 84,5% (из 71 умерло 11 пациентов) – без статистически значимой разницы (p = 0,12), то в 3-й – 66,1% (из 62 умерло 21), что существенно различалось c 1-й и 2-й группами (p = 0,0003 и p = 0,023 соответственно). Однако за исследуемый период медиана ОВ не достигнута.
Была исследована связь общей выживаемости с рядом факторов. Методом множественной регрессии установлено влияние объема (R = 0,183; p = 0,036; n = 130) и числа перелитых доз (R = 0,162; p = 0,029; n = 190) донор ских эритроцитов, а также низкого прироста уровня гемоглобина (R =–0,180; p = 0,017; n = 190) на общую выживаемость пациентов. Это указывает на тот факт, что чем более длительно купируется анемия у больного и чем выше потребность в переливаниях донорских эритроцитов для адекватной коррекции анемии, тем хуже прогноз основного заболевания, что позволяет стратифицировать больных на группы риска. В группе больных низкого риска (с полным ответом на переливания донорских эритроцитов – уровень гемоглобина повышался на ×10 г/л) общая выживаемость составила 94,7%. В группе пациентов промежуточного риска (частичный ответ – уровень Hb повышался на 5–9,9 г/л) общая выживаемость констатирована в 84,5%; в группе больных высокого риска (минимальный ответ – уровень Hb повышался на <5 г/л) общая выживаемость – 66,1%.
В группе больных низкого риска (с полным ответом на переливания донорских эритроцитов – уровень гемоглобина повышался на ×10 г/л) общая выживаемость составила 94,7%. В группе пациентов промежуточного риска (частичный ответ – уровень Hb повышался на 5–9,9 г/л) общая выживаемость констатирована в 84,5%; в группе больных высокого риска (минимальный ответ – уровень Hb повышался на <5 г/л) общая выживаемость – 66,1%.
В то же время не выявлено связи общей выживаемости в течение 4 месяцев ни с возрастом пациентов (R = 0,05; p = 0,51; n = 190), ни с полом (R = 0,011; p = 0,89; n = 186), ни с исходным содержанием гемоглобина (R = 0,017;
p = 0,81; n = 190).
Обсуждение
Анемия при гемобластозах нередко выступает ведущим симптомом заболевания (в 20–98% случаев), снижает противоопухолевый эффект химиотерапии, ухудшает прогноз и качество жизни пациентов [2–7, 19]. В период постановки диагноза при лимфогранулематозе анемия выявляется у 22% больных, увеличиваясь на фоне противоопухолевого лечения до 54,5%; при НХЛ – у 34,9%, увеличиваясь на фоне ХТ до 73,7%; при ХЛЛ – у 30,1%, повышаясь до 72,9%; при ММ – у 56%, возрастая до 77,4% [6, 7]. Еще чаще анемию выявляют у пациентов с острыми миелоидными и лимфоидными лейкозами, МДС. При первичной диагностике ПМФ анемия встречается у 38% пациентов с постепенным возрастанием частоты в процессе прогрессирования заболевания; при эссенциальной тромбоцитемии в фазе бластного криза – у 74% больных; при ХМЛ на фоне терапии ингибиторами тирозинкиназы – от 40 до 83% [5, 19–23]. Причем анемия у больных индолентными формами лимфопролиферативных заболеваний нередко расценивается в качестве «индикатора» для начала ХТ [24].
Еще чаще анемию выявляют у пациентов с острыми миелоидными и лимфоидными лейкозами, МДС. При первичной диагностике ПМФ анемия встречается у 38% пациентов с постепенным возрастанием частоты в процессе прогрессирования заболевания; при эссенциальной тромбоцитемии в фазе бластного криза – у 74% больных; при ХМЛ на фоне терапии ингибиторами тирозинкиназы – от 40 до 83% [5, 19–23]. Причем анемия у больных индолентными формами лимфопролиферативных заболеваний нередко расценивается в качестве «индикатора» для начала ХТ [24].
При выборе тактики корригирующего анемию лечения таких больных необходимо учитывать риск развития опасных для жизни осложнений, возникающих вследствие действия хронической гипоксии из-за неадекватной оксигенации жизненно важных органов, прежде всего мозга, сердца, печени, а также механизмы развития анемии, с учетом которых можно купировать анемию или значительно улучшить общее состояние пациента. У больных онкогематологическими заболеваниями в генезе анемии могут принимать участие сразу несколько факторов: а) опухолевая инфильтрация КМ с вытеснением эритроидных элементов; б) гемолиз эритроцитов; в) супрессия эритроидного ростка провоспалительными цитокинами; г) низкая продукция эндогенного эритропоэтина; д) функциональный дефицит железа вследствие повышения продукции гепсидина; е) свободнорадикальное окисление фосфолипидов клеточных мембран во время проведения ХТ; ж) геморрагический синдром [3, 25–30]. С учетом выявления факторов, участвующих в развитии анемии, в настоящее время возможна ее коррекция патогенетическими методами, например, назначением препаратов эритропоэтина [1, 3]. Однако не для всех пациентов патогенетическая терапия может быть приемлема, ввиду того что эффективность ее, как правило, не превышает 60–70%, а ответ на терапию ожидается через 2–3 месяца [25, 31]. Выжидательная тактика для больных гемобластозами не всегда оправдана вследствие опасности прогрессирования опухолевого процесса и риска для жизни пациента от гипоксии миокарда и других жизненно важных органов, особенно в пожилом возрасте с наличием сопутствующей ишемической болезни сердца. В то же время ТЭ являются универсальным и срочным методом коррекции анемии, независимо от нозологической формы болезни. Следовательно, заместительная гемокомпонентная терапия остается приоритетной, тем более при угрозе жизни больного, так как она позволяет в кратчайшие сроки добиться улучшения общего состояния пациента.
С учетом выявления факторов, участвующих в развитии анемии, в настоящее время возможна ее коррекция патогенетическими методами, например, назначением препаратов эритропоэтина [1, 3]. Однако не для всех пациентов патогенетическая терапия может быть приемлема, ввиду того что эффективность ее, как правило, не превышает 60–70%, а ответ на терапию ожидается через 2–3 месяца [25, 31]. Выжидательная тактика для больных гемобластозами не всегда оправдана вследствие опасности прогрессирования опухолевого процесса и риска для жизни пациента от гипоксии миокарда и других жизненно важных органов, особенно в пожилом возрасте с наличием сопутствующей ишемической болезни сердца. В то же время ТЭ являются универсальным и срочным методом коррекции анемии, независимо от нозологической формы болезни. Следовательно, заместительная гемокомпонентная терапия остается приоритетной, тем более при угрозе жизни больного, так как она позволяет в кратчайшие сроки добиться улучшения общего состояния пациента.
Показаниями для ТЭ служат выраженная клиническая картина анемии и снижение содержания гемоглобина и гематокрита. В настоящее время существуют две тактики: рестриктивная, при которой переливания донорских эритроцитов проводят при содержании гемоглобина менее 70 г/л, поддерживая его в пределах 70–90 г/л, и либеральная – переливания эритроцитов осуществляют при содержании гемоглобина менее 100 г/л [32]. Выбирая одну или другую тактику коррекции хронической анемии у больных гемобластозами, необходимо тщательно взвесить потенциальный риск и выгоду от гемотрансфузий. Так, несмотря на возросшие требования к отбору доноров, использованию высокотехнологичных методов диагностики трансмиссивных инфекций, индивидуальному подбору доноров, тем не менее сохраняется риск передачи инфекций (вирусные гепатиты В, С, ВИЧ и др.) от донора реципиенту, аллоиммунизация пациента антигенами, а также риск перегрузки организма железом с развитием гемосидероза внутренних органов [8–12, 14, 15]. В связи с этим в последние годы у пациентов с хронической анемией донорские эритроциты переливают только для коррекции важнейших симптомов анемии, не поддающихся основной патогенетической терапии [15].
В настоящее время существуют две тактики: рестриктивная, при которой переливания донорских эритроцитов проводят при содержании гемоглобина менее 70 г/л, поддерживая его в пределах 70–90 г/л, и либеральная – переливания эритроцитов осуществляют при содержании гемоглобина менее 100 г/л [32]. Выбирая одну или другую тактику коррекции хронической анемии у больных гемобластозами, необходимо тщательно взвесить потенциальный риск и выгоду от гемотрансфузий. Так, несмотря на возросшие требования к отбору доноров, использованию высокотехнологичных методов диагностики трансмиссивных инфекций, индивидуальному подбору доноров, тем не менее сохраняется риск передачи инфекций (вирусные гепатиты В, С, ВИЧ и др.) от донора реципиенту, аллоиммунизация пациента антигенами, а также риск перегрузки организма железом с развитием гемосидероза внутренних органов [8–12, 14, 15]. В связи с этим в последние годы у пациентов с хронической анемией донорские эритроциты переливают только для коррекции важнейших симптомов анемии, не поддающихся основной патогенетической терапии [15].
Однако при онкогематологических заболеваниях больные отличаются нестабильностью общего соматического состояния и вариабельностью течения основного опухолевого процесса, они получают цитостатическую терапию, обладающую токсичностью не только на гемопоэз, но и на другие жизненно важные органы и системы, включая сердечно-сосудистую, что приводит к снижению толерантности организма к гипоксии [2, 16]. Поэтому рестриктивная тактика в отношении переливаний эритроцитов у такой категории пациентов, особенно в пожилом возрасте с наличием сопутствующей сердечной недостаточности, небезопасна.
В проведенной работе продемонстрировано, что у 30% онкогематологических больных получен полный ответ на переливания эритроцитов, а прирост содержания Hb составил более 10 г/л; у них быстро происходило восстановление собственного гемопоэза после курсов противоопухолевой терапии и сохранялся эффект от переливаний эритроцитов на длительный период. У таких пациентов без признаков сердечной недостаточности коррекцию анемии проводили при уровне Hb <80 г/л. Стабильного состояния достигали после переливания 2,9 ± 0,2 дозы эритроцитов. У 37,4% больных с частичным ответом также отмечался удовлетворительный эффект от ТЭ с приростом гемоглобина на одну перелитую дозу эритроцитов 5–9,7 г/л. Улучшение состояния в этой группе больных достигалось за счет переливания 4,5 ± 0,3 дозы эритроцитов. Как в первой, так и во второй группе пациентов содержание гемоглобина через 10–14 дней снижалось незначительно. В то же время недостаточная эффективность от переливаний донорских эритроцитов наблюдалась в третьей группе с минимальным ответом. Прирост уровня Hb на одну перелитую дозу эритроцитов констатирован менее 5 г/л. Улучшение состояния и повышение концентрации Hb >80 г/л у таких пациентов удавалось достичь лишь после переливания 6,4 ± 0,8 дозы донорских эритроцитов. У этих больных выявлялись не только продвинутая стадия заболевания с депрессией эритропоэза, обусловленной прогрессированием опухолевого процесса и токсическим эффектом цитостатической терапии, но нередко и гемолиз эритроцитов, как проявление основного заболевания.
При определении тактики заместительной гемокомпонентной терапии следует учитывать также возраст пациентов и наличие сердечной или дыхательной патологии в связи с риском гипоксических осложнений. У пациентов пожилого возраста, даже при более высоких показателях периферической крови (содержание гемоглобина 80–100 г/л, гематокрита 26–30%), чаще наблюдались тахикардия (пульс свыше 90–110 уд/мин), гипотония (артериальное давление менее 120/70 мм рт. ст.), одышка при умеренной нагрузке, а иногда и в покое. В то же время после переливания эритроцитов у них отмечалось значительное улучшение общего состояния и купирование или значительное уменьшение клинической симптоматики. Поэтому для коррекции анемии у пожилых больных, а также у пациентов с наличием сердечной или легочной недостаточности, с признаками неэффективного эритропоэза, переливания эритроцитов необходимо проводить при содержании Hb <90–95 г/л и уровне гематокрита <30%.
При заместительной терапии анемии с помощью гемотрансфузий мы учитывали не только показатели периферической крови, но и генез ее развития. В ходе исследования выявлено, что основными причинами анемии были опухолевая инфильтрация КМ, нарушение гемопоэза, гемолиз эритроцитов, а также токсическое действие ХТ. В то же время у некоторых больных выявлялся дефицит железа, геморрагический синдром, обусловленный ДВС-синдромом и/или тромбоцитопенией. Поэтому таким пациентам помимо переливаний донорских эритроцитов назначали препараты железа; для остановки кровотечения больные получали свежезамороженную плазму, концентрат тромбоцитов в комплексе с гемостатическими препаратами. В последние годы для коррекции анемии, прежде всего обусловленной токсическим эффектом противоопухолевой терапии, а также отрицательным действием опухолевых клеток на эритропоэз, большое внимание уделяется патогенетической терапии с назначением эритропоэзстимулирующих агентов. Их применение позволяет добиться положительного результата у 24–85% больных [1, 25, 31]. Эритропоэзстимулирующая терапия особенно эффективна, если анемия обусловлена низким синтезом эндогенного эритропоэтина [1, 3, 31]. Тем не менее больные, имеющие тяжелую степень анемии с уровнем Hb <80 г/л, Ht <25%, нуждаются в ТЭ, даже если им проводится терапия препаратами рекомбинантного эритропоэтина.
Анемия, трудно поддаваемая коррекции с помощью переливаний донорских эритроцитов, часто была вызвана гемолизом, не позволяющим добиться повышения уровня гемоглобина и гематокрита до необходимых цифр. У этих больных наблюдалось повышение непрямого билирубина (19,2–41,9 мкмоль/л). В качестве патогенетической терапии таким пациентам показано назначение кортикостероидных гормонов и иммуносупрессивных препаратов, что ранее было показано нами у пациента с НХЛ с синдромом Эванса, получившего более 60 переливаний донорских эритроцитов и пролеченного глюкокортикоидными гормонами без эффекта. Однако был получен положительный ответ на применение анти-CD20 моноклональных антител (ритуксимаба) с последующей длительной ремиссией [33].
Необходимо также отметить, что общая выживаемость в течение 4 месяцев от начала трансфузионной терапии существенно отличалась в группе с минимальным ответом на переливания донорских эритроцитов (рис. 2), составляя 66,1% против 94,7 и 84,5% соответственно в группах с полным и частичным ответами. Это подтверждает ту версию, что чем труднее купируется анемия у пациента, т. е. чем ниже эффективность ТЭ, тем хуже прогноз основного заболевания, что позволяет стратифицировать больных на группы риска. В группе больных низкого риска (с полным ответом на ТЭ – уровень гемоглобина повышался на 10 г/л) общая выживаемость составила 94,7%. В группе пациентов промежуточного риска (частичный ответ — уровень Hb повышался на 5–9,9 г/л) ОВ – 84,5%; в группе больных высокого риска (минимальный ответ – уровень Hb повышался на <5 г/л) ОВ – 66,1%. Стратификация пациентов на группы риска может быть взята в качестве
прогностического маркера.
Таким образом, основными причинами анемии у проанализированных больных явились выраженная депрессия эритропоэза, обусловленная проявлением опухолевого заболевания, токсическим действием химиотерапии, гемолизом эритроцитов, а также дефицитом железа и геморрагическим синдромом. Заместительные переливания эритроцитов позволяют корригировать анемию, восстановить уровень гемоглобина и гематокрита у большинства пациентов. Однако после прекращения переливаний возможно снижение уровня гемоглобина, что требует повторных трансфузий. Стратификация пациентов на группы риска в зависимости от эффективности пере-
ливания донорских эритроцитов позволяет прогнозировать течение основного заболевания и дифференцированно подходить к терапии анемии при гемобластозах.
Литература
1. Бессмельцев С.С., Романенко Н.А., Абдулкадыров К.М. Современные подходы к лечению анемии у больных с онкогематологическими заболеваниями // Современная онкология. – 2010. – Т. 12, № 1. – С. 70–75.
2. Oliva E.N., Dimitrov B.D., Benedetto F. et al. Hemoglobin level threshold for cardiac remodeling and quality of life in myelodysplastic syndrome // Leuk. Res. – 2005. – Vol. 29. – P. 1217–1219.
3. Романенко Н.А. Патогенез и терапия анемии препаратами рекомбинантного эритропоэтина у онкогематологических больных (обзор литературы) // Онкогематология. – 2012. – № 3. – С. 20–29.
4. Moullet I., Salles G., Ketterer N. et al. Frequency and significance of anemia in non-Hodgkin’s lymphoma patients // Ann Oncol. – 1998. – Vol. 9. – P. 1109–1115. 5. Santos F.P., Alvarado Y., Kantarjian H. et al. Long-term prognostic impact of the use of erythropoietic-stimulating agents in patients with chronic myeloid leukemia in chronic phase treated with imatinib // Cancer. 2011. – Vol. 117, № 5. – P. 982–991.
6. Steurer M., Wagner H., Gastel G. Prevalence and management of anaemia in haematologic cancer patients receiving cyclic nonplatinum chemotherapy: results of a prospective national chart survey // Wien. Klin. Wochenschr. – 2004. – Vol. 116, № 11–12. – P. 367–372.
7. Truong P.T., Parhar T., Hart J. et al. Population-based analysis of the frequency of anemia and its management before and during chemotherapy in patients with malignant lymphoma // Am. J. Clin. Oncol. – 2010. – Vol. 33, № 5. – P. 465–468.
8. Грицаев С.В., Даваасамбуу Б., Романенко Н.А., Абдулкадыров К.М. Отбор больных для терапии хелаторами железа // Клин. онкогематология. – 2013. – Т. 6, № 2. – С. 204–209.
9. Brecher M.E., Hay S.N. Bacterial contamination of blood components // Clin. Microbiol. Rev. – 2005. – Vol. 18, № 1. – P. 195–204.
10. Dreyfus F. The deleterious of iron overload in patients with myelodysplastic syndromes // Blood Rev. – 2008. – Vol 22, Suppl. 2 – S. 29–34.
11. Khorana A.A., Francis C.W., Blumberg N. et al. Blood Transfusions, Thrombosis, and Mortality in Hospitalized Patients With Cancer // Arch. Intern. Med. – 2008. – Vol. 168, № 21. — P. 2377–2381.
12. Leitch H.A., Vickars L.M. Supportive care and chelation therapy in MDS: are we saving lives or just lowering iron? // Hematology Am. Soc. Hematol. Educ. Program. – 2009. – P. 664–672.
13. Жибурт Е.Б., Караваев А.В., Шестаков Е.А. и др. Правила переливания эритроцитов, основанные на доказательствах // Трансфузиология. – 2012. – Т. 13, № 3. – C. 55.
14. Правила клинического использования донорской крови и (или) ее компонентов // Приказ от 2 апреля 3013 г. № 183н «Об утверждении правил клинического использования донорской крови и (или) ее компонентов» [Электронный ресурс] // http://www.transfusion. ru/2013/08-29-1.pdf.
15. Инструкция по применению компонентов крови (Утверждена Приказом Минздрава РФ от 25 ноября 2002 года № 363 «Об утверждении Инструкции по применению компонентов крови») // [Электронный ресурс]// http://www.zdrav.ru/library/regulations/detail.php?ID = 26150.
16. Романенко Н.А. Терапия и профилактика анемии и перегрузки железом у больных миелодиспластическим синдромом // Биомедицинский журнал. – WWW.Medline.ru. – 2013. – Т. 13. – С. 967–986.
17. Техническое руководство американской ассоциации банков крови / Под ред. Ю.Н. Токарева. – Милан: Европейская школа трансфузионной медицины, 2000. – 1056 с.
18. Romanenko N.A. Study of efficacy red cell transfusions and their influencing on quality of life in hematological malignancies patients with anemia // Haematologica – The Hematology journal. – 2012. – Vol. 97, Suppl. 1. – P. 163.
19. Quintás-Cardama A., De Souza Santos F.P., Kantarjian H. et al. Dynamics and management of cytopenias associated with dasatinib therapy in patients with chronic myeloid leukemia in chronic phase after imatinib failure // Cancer. – 2009. – Vol. 115, № 17. – P. 3935–3943.
20. Tefferi A., Lasho T.L., Jimma T. et al. One thousand patients with primary myelofibrosis: the mayo clinic experience // Mayo Clin. Proc. – 2012. – Vol. 87, № 1. – P. 25–33.
21. Passamonti F., Rumi E., Arcaini L. et al. Blast phase of essential thrombocythemia: A single center study // Am. J. Hematol. – 2009. – Vol. 84, № 10. – P. 641–644.
22. Романенко Н.А., Абдулкадыров К.М., Бессмельцев С.С. Эффективность коррекции анемии у больных хроническим миелолейкозом, развившейся на фоне терапии иматинибом // Биомедицинский журнал. – WWW.Medline.ru. – 2010. – Т. 11. – С. 376–389.
23. Cortes J., O’Brien S., Quintas A. et al. Erythropoietin is effective in improving the anemia induced by imatinib mesylate therapy in patients with chronic myeloid leukemia in chronic phase // Cancer. – 2004. –Vol. 100, № 11. – P. 2396–2402. 24. Samuelsson J. Long-standing resolution of anemia in symptomatic low-grade non-Hodgkin’s lymphoma patients treated with recombinant human erythropoietin as sole therapy // Med. Oncol. – 2002. – Vol. 19, № 1. – P. 69 72.
25. Романенко Н.А., Абдулкадыров К.М. Патогенетическая коррекция анемии эритропоэзстимулирующими препаратами у больных лимфопролиферативными заболеваниями // Онкогематология. – 2011. – № 3. – С. 39–49.
26. Рукавицын О.А. Актуальные вопросы диагностики и лечения анемии при хронических заболеваниях // Клинич. онкогематол. – 2012. – Т. 5, № 4. – С. 296–304.
27. Eve H.E., Rule S.A. Autoimmune haemolytic anaemia associated with mantle cell lymphoma // Int. J. Hematol. – 2010. – Vol. 91, № 2. – P. 322–325.
28. Romanenko N.A., Rozanova O.E., Glazanova T.V., Abdulkadyrov K.M. Role of cytokines in resistance to erythropoiesis stimulating agents treatment of anaemia in patients with lymphoproliferative disorders // Haematologica. – 2012. – Vol. 97, Suppl. 1. – P. 550–551.
29. Tsopra O.A., Ziros P.G., Lagadinou E.D. et al. Disease-related anemia in chronic lymphocytic leukemia is not due to intrinsic defects of erythroid precursors: a possible pathogenetic role for tumor necrosis factor-alpha // Acta Haematol. – 2009. – Vol. 121, № 4. – P. 187–195.
30. Zupanić-Krmek D., Lang N., Jurcić D. et al. Analysis of the influence of various factors on anemia in patients with lymphoid malignancies // Acta Clin. Croat. – 2011. – Vol. 50, № 4. – P. 495–500.
31. Романенко Н.А., Бессмельцев С.С., Беркос М.В. и др. Прогностическая значимость ряда лабораторных показателей крови при использовании препаратов, стимулирующих эритропоэз у больных лимфопролиферативными заболеваниями с анемией // Тер. архив. – 2013. – Т. 85, № 8. – С. 81–86.
32. Жибурт Е.Б., Шестаков Е.А. Внедрение правил назначения компонентов крови в клиническую практику // Трансфузиология. – 2007. – Т. 8, № 3–4. – С. 47–59.
33. Романенко Н.А., Бессмельцев С.С., Абдулкадыров К.М. Патогенетическое лечение пациентки с неходжкинской лимфомой маргинальной зоны селезенки, осложненной синдромом Эванса // Каз. мед. журн. – 2012. – Т. XCIII, № 5. – С. 843–846.
Концентрация гемоглобина и ферритина у младенцев в возрасте 8 месяцев
Цель:
Чтобы определить оптимальный возраст для скрининга на дефицит железа, было исследовано нормальное распределение гемоглобина и ферритина в репрезентативной выборке населения.
Методы:
Нормальные значения гемоглобина и ферритина были измерены на образцах капилляров пятки, взятых из репрезентативной когорты из 1175 младенцев в возрасте 8 месяцев, которые были случайным образом отобраны из детей, принимавших участие в Продольном исследовании беременности и детства Avon (ALSPAC).
Результаты:
Гемоглобин был нормально распределен: среднее (SD) 117 (11) миллиграммов, 95% доверительный интервал (CI) от 116 до 118 и диапазон 72-153 миллиграммов. Ферритин имел нормальное логарифмическое распределение: среднее геометрическое 38,5 мкг / л, 95% ДИ 37,0–39,9, диапазон 7,1–224 мкг / л. Пятый центиль для гемоглобина составлял 97 миллиграммов, а для ферритина — 16,9 микрограмм / л. Корреляции между гемоглобином и ферритином не обнаружено.Множественный регрессионный анализ показал, что концентрация ферритина положительно связана с массой тела при рождении (p <0,0001) и полом ребенка (девочки с более высокими концентрациями) (p <0,0001), но отрицательно с массой ребенка в 8 месяцев (p <0,0001). Концентрация гемоглобина положительно зависела от веса ребенка в 8 месяцев (p = 0,04). Концентрации ни гемоглобина, ни ферритина не были связаны с социальным классом, измеряемым уровнем образования матери.
Вывод:
Эти данные определяют нормальный диапазон гемоглобина и ферритина в образцах капилляров в популяции Великобритании и позволяют предположить, что анемия часто встречается в младенчестве.Используя текущие рекомендации, 23% младенцев будут идентифицированы как страдающие анемией. Для британских младенцев в возрасте 8 месяцев более репрезентативным «порогом» для анемии была бы концентрация гемоглобина <97 миллиграммов, а для железодефицитного ферритина <16 микрограмм / л.
Уровни гемоглобина во время беременности
Наша цель FirstCry Parenting — предоставить вам наиболее полную, точную и актуальную информацию.
Каждая статья, которую мы публикуем, соответствует строгим правилам и включает несколько уровней рецензирования, как нашей редакционной командой, так и экспертами.Мы приветствуем ваши предложения по повышению полезности этой платформы для всех наших пользователей. Напишите нам по адресу [email protected]
.
Последнее обновление:
Исследователи считают, что около 20% беременных женщин во всем мире страдают анемией или низким уровнем гемоглобина. Анемия во время беременности увеличивает вероятность таких проблем, как материнская и перинатальная смертность, преждевременные роды и низкая рождаемость.
Что такое гемоглобин?
Гемоглобин — это сложный белок крови, который помогает транспортировать кислород и углекислый газ к различным частям тела.Железо является основным компонентом красных кровяных телец, отсюда и название гемоглобин — «гемо» означает железо, а «глобулин» — это название белка. Уровень гемоглобина у женщин должен составлять от 12 до 16 г / дл.
Важность гемоглобина во время беременности
Когда женщина беременна, ей нужно больше кислорода, чем обычно, так как плод также нуждается в кислороде. Следовательно, как только женщина беременеет, оценивается ее уровень гемоглобина — кислородная способность крови напрямую зависит от концентрации циркулирующего гемоглобина.
Нормальный диапазон гемоглобина
Гемоглобин измеряется в г / дл (грамм на децилитр). Вот нормальный уровень гемоглобина у взрослых.
- При отсутствии беременности: от 12 до 15,8 г / дл или от 120 до 158 г / л
- I триместр беременности: от 11,6 до 13,9 г / дл или от 116 до 139 г / л
- 2 — триместр беременности: от 9,7 до 14,8 г / дл или от 97 до 148 г / л
- 3 -й триместр беременности: от 9,5 до 15 г / дл или от 95 до 150 г / л
Почему уровень гемоглобина падает во время беременности?
Ожидается снижение гемоглобина во время беременности.На самом деле, снижение гемоглобина до 10,5 г / дл во время беременности считается нормальным. Причина этого довольно проста — когда женщина беременна, объем ее крови увеличивается на 50%, чтобы обеспечить развивающегося ребенка необходимыми питательными веществами. К 8 -й неделе беременности уровень в плазме крови выше, чем у будущей матери. Из-за снижения концентрации эритроцитов в крови уровень гемоглобина падает до 10,5 г / дл. Все, что ниже этого, требует внимания.
Эффекты низкого уровня гемоглобина
Уровень гемоглобина ниже 10,5 г / дл может повлиять на здоровье беременной женщины. Следовательно, важно принимать добавки железа во время беременности в соответствии с рекомендациями врача. Вот несколько побочных эффектов низкого уровня гемоглобина во время беременности:
- Вы почувствуете себя измученным
- Головокружение станет нормальным
- Ваша кожа и губы побледнеют
- Вы почувствуете одышку даже во время отдыха.
- У вас будет учащенное сердцебиение
- Ваши руки и ноги часто будут мерзнуть
- Ваши ногти станут ломкими и легко сломаются
Это состояние может ухудшиться при дальнейшем падении гемоглобина.Если гемоглобин упадет до 6 г / дл, то у будущей мамы может быть стенокардия. В этом состоянии беременная женщина будет испытывать сильную боль в груди, которая медленно переходит в руки, плечи и шею из-за недостаточного притока крови к сердцу.
Есть ли у вас риск снижения гемоглобина?
Как упоминалось ранее, небольшое снижение гемоглобина во время беременности — это нормально. Но если вы вступаете в беременность на стадии, когда ваш гемоглобин уже ниже нормы, тогда у вас может быть более высокий риск снижения гемоглобина во время беременности.Некоторые из факторов до беременности, которые могут способствовать такому состоянию низкого гемоглобина у женщины:
- Потеря большого количества крови во время менструации, особенно в последний цикл перед беременностью
- Соблюдение диеты с низким содержанием железа
- Сдал кровь незадолго до беременности
- Неадекватное поглощение железа
- Забеременеть вскоре после последних родов
Существует 3 типа проблем с гемоглобином, с которыми вы можете столкнуться во время беременности:
- Железодефицитная анемия — это происходит, когда в организме не хватает железа для производства оптимального гемоглобина.
- Анемия с дефицитом фолиевой кислоты — Организм нуждается в фолиевой кислоте для производства большего количества эритроцитов, которые помогают транспортировать кислород к тканям тела. Недостаточное количество зеленых листовых овощей может вызвать проблемы с гемоглобином, связанные с фолиевой кислотой.
- Дефицит витамина B12 — Организм также нуждается в достаточном количестве витамина B12 для образования здоровых красных кровяных телец. Отсутствие витамина в диете может вызвать проблемы, которые напрямую влияют на уровень гемоглобина.
Как повысить гемоглобин при беременности
Поскольку мы знаем, что уровень гемоглобина, скорее всего, снизится во время беременности, вы должны проконсультироваться с врачом и принимать добавки железа.Кроме того, изменение диеты может помочь вам восполнить запасы железа, фолиевой кислоты, витамина B12 и витамина C, без которых у вас может возникнуть дефицит гемоглобина.
Вот список продуктов, которые могут помочь вам восполнить пробел.
- Вы должны включать в свой рацион листовые овощи, такие как палак, мети, сухих фруктов, пищевые зерна, такие как ячмень, кукурузное просо и семена кунжута. Это надежные источники железа.
- Фрукты, богатые железом, такие как гуава, киви, персики, инжир, яблоки и т. Д.незаменимы в вашем повседневном рационе.
- Пища, богатая витамином С, должна быть включена в ваш рацион, так как она помогает организму усваивать железо. Такие фрукты, как киви, апельсин, лайм и малина, являются отличными источниками витамина С. Темная зелень, сладкий перец, брокколи и помидоры также богаты витамином С и должны быть включены в ваш рацион.
- Комплекс фолиевой кислоты и витамина B помогает в производстве красных кровяных телец, которые, в свою очередь, повышают уровень гемоглобина в организме.Поэтому продукты, богатые фолиевой кислотой и комплексом витаминов B, такие как авокадо, окра, салат, репа, ростки и т. Д., Также должны быть частью вашего ежедневного приема пищи.
- Было замечено, что избыточное потребление кальция, глютена и кофеина может блокировать усвоение железа организмом. Следовательно, во время беременности необходимо ограничить потребление:
- Кофе / чай
- Спирт
- Макаронные изделия и продукты из пшеницы (глютен)
- Петрушка (щавелевая кислота)
- Молочные продукты
Когда уровень гемоглобина становится высоким во время беременности?
Уровни гемоглобина во время беременности могут возникать из-за заболеваний сердца, легких и почек.Гемоглобин у беременной также может повышаться из-за:
1. Обезвоживание
Если во время беременности потребление жидкости или воды уменьшается, может наблюдаться резкое повышение гемоглобина. То же самое происходит с увеличением потребления жидкости.
2. Эритроцитоз
В этом состоянии наблюдается резкий рост красных кровяных телец. Во время беременности, если по какой-то причине организм не может удовлетворить потребность различных тканей в кислороде, происходит увеличение выработки красных кровяных телец.Это, очевидно, увеличивает уровень гемоглобина в организме.
3. Передозировка препаратов железа
Повышение уровня железа в организме приводит к внезапному повышению уровня гемоглобина. Следовательно, не принимайте добавки железа без консультации с врачом.
Эффекты высокого уровня гемоглобина
Вы можете быть удивлены, но высокий уровень гемоглобина во время беременности может быть довольно опасным. Вот некоторые нежелательные последствия высокого гемоглобина во время беременности:
- Увеличивает шансы на низкую массу тела при рождении или LBW
- В течение триместра 1 и 2 может привести к SGA плода (малый для гестационного возраста)
- Если уровень гемоглобина превышает 14 г / дл в течение 2 — триместра, это может указывать на преэклампсию
- Увеличение толщины крови может напрямую влиять на кровоток в организме матери.В результате кровь может не достигать плаценты, что, очевидно, будет препятствовать здоровому развитию ребенка.
Лечение высокого уровня гемоглобина
Не существует прописанных домашних средств от высокого уровня гемоглобина во время беременности. К этому должен относиться эксперт по своему усмотрению. За вами будет внимательно наблюдать специалист, который определит схему лечения на основе ваших симптомов.
Чтобы в полной мере насладиться беременностью, следите за тем, что вы едите, прислушивайтесь к своему телу и особенно к своему врачу.В случае малейших сомнений немедленно обратитесь к врачу.
Ресурсы и ссылки: WebMD
Также читайте: Железодефицитная анемия во время беременности
Кормление грудью и анемия: будьте осторожны
Исследование анемии и дефицита железа у 9-месячных младенцев Джеймса Бэй Кри, о котором сообщается в этом выпуске (стр. 323) 1, поднимает 2 интересных и провокационных вопроса. Во-первых, что такое анемия в этой возрастной группе? Во-вторых, насколько хорошо 9-месячный ребенок, находящийся на грудном вскармливании, защищен от дефицита железа?
Обычно используемые нормы были получены из популяций белых детей некоренного происхождения, живущих вблизи уровня моря 2, но эти пороговые значения, по-видимому, не применимы ко всем группам населения.Эмонд и его коллеги3 обнаружили, что для британских детей более репрезентативным порогом анемии была концентрация гемоглобина менее 97 г / л. Другие исследователи4 обнаружили, что у афроамериканцев средний уровень гемоглобина может быть на 5 г / л ниже, чем средний уровень для белых людей, хотя следует проявлять осторожность, делая выводы из этих различий.5 В текущем исследовании только 5,3% Младенцы на искусственном вскармливании, большинство из которых получали смесь, обогащенную железом, имели концентрацию гемоглобина ниже 105 г / л в возрасте 9 месяцев, и ни у одного из них не наблюдался значительный микроцитоз.Могут ли уровни для этой группы младенцев, вскармливаемых смесью, представлять «нормальный» диапазон для младенцев из племени кри Джеймс Бэй? Напротив, как у детей, вскармливаемых грудью, так и у детей, которых кормили коровьим молоком, были обнаружены признаки дефицита железа. В общей сложности у 31% детей, вскармливаемых грудью, уровень гемоглобина был ниже 105 г / л, а у 17% — ниже 100 г / л, по сравнению с 5% и 1% соответственно среди детей, вскармливаемых смесью. Кроме того, отношение шансов для микроцитоза (средний объем клеток менее 71 мкл) было в 11 раз выше среди младенцев, находящихся на грудном вскармливании, чем среди их аналогов на искусственном вскармливании.Микроцитарная гипохромная анемия у этих младенцев, скорее всего, была вызвана дефицитом железа, хотя другие, менее вероятные состояния, такие как хроническое заболевание, дефицит витамина B 6 , отравление свинцом и малая талассемия, могут дать аналогичную картину. Повышенная потребность в железе среди детей, находящихся на грудном вскармливании, по сравнению с детьми, вскармливаемыми смесью, вряд ли была фактором. Средняя прибавка в весе и, следовательно, увеличение объема крови с ростом у младенцев, вскармливаемых грудью, были меньше. Во всяком случае, это должно было привести к снижению спроса на железо и уменьшению причин его дефицита.
Дефицит железа, связанный с потреблением коровьего молока, хорошо известен. Дефицит железа у младенцев, находящихся на грудном вскармливании, воспринимается хуже, 6 однако результаты этого исследования показывают, что он может возникать к 9-месячному возрасту. Здоровый ребенок защищен от дефицита железа в течение первых 6 месяцев жизни. Уровни гемоглобина при рождении высоки, в диапазоне от 180 до 210 г / л, а гемоглобин содержит около 75% запасов железа новорожденного. Теряется очень мало железа, поэтому доношенный ребенок весом 3,5 кг, который удвоил свой вес к 6 месяцам, должен иметь возможность поддерживать уровень гемоглобина от 90 до 110 г / л без необходимости в дополнительном железе.После этого экзогенные источники железа становятся важными, и, возможно, именно здесь и начинается проблема. Младенец набирает около 3,5 кг в возрасте от 6 до 12 месяцев, и для поддержания концентрации гемоглобина 110 г / л требуется около 1 мг / сут дополнительного железа. Грудное молоко содержит от 0,3 до 0,5 мг железа на литр. Даже если до 50% этого железа усваивается, этого может быть недостаточно, и могут потребоваться дополнительные источники пищевого железа, чтобы предотвратить истощение запасов железа и анемию. Обогащенные железом злаки, которые являются важными источниками железа, могут не использоваться или могут быть недоступны в отдаленных общинах.Другие факторы могли способствовать дефициту железа у детей, находящихся на грудном вскармливании, в этом исследовании. Влияет ли дефицит железа у матери на уровень железа у младенцев и концентрацию железа в грудном молоке? Давали ли младенцу на грудном вскармливании чай или продукты, содержащие такие вещества, как фитаты, которые могут мешать усвоению железа?
Это важное исследование имеет значение для программ общественного здравоохранения и питания, особенно в отношении грудного вскармливания и введения дополнительных продуктов питания.Предлагать улучшить грудное молоко — все равно что попасть в минное поле: нужно действовать осторожно. Важно, чтобы эти результаты не истолковывались как критика грудного вскармливания. Грудь по-прежнему самая лучшая. Однако из-за серьезных, иногда необратимых неврологических эффектов и эффектов развития, которые могут быть связаны с железодефицитной анемией, эти результаты нельзя игнорировать. Необходимы дальнейшие исследования. Между тем, кажется разумным снабдить детей грудного вскармливания после 6 месяцев 7 дополнительными источниками железа 7 либо в виде продуктов, обогащенных железом (например,g., детские каши) или, если истощение серьезное, как дополнительное железо.
Конкурирующие интересы: не заявлены.
Уровни гемоглобина в первом триместре беременности связаны с риском гестационного сахарного диабета, преэклампсии и преждевременных родов у китайских женщин: ретроспективное исследование | BMC Беременность и роды
В этом большом исследовании беременных мы обнаружили, что женщины, у которых до беременности ИМТ был ≥24 кг / м 2 , имели значительно более высокие уровни Hb в первом триместре, чем женщины, у которых до беременности ИМТ был ниже. <24 кг / м 2 .Кроме того, у женщин, у которых впоследствии развился ГСД и ПЭ, уровень гемоглобина в первом триместре был значительно выше, чем в контрольной группе, тогда как у женщин с преждевременными родами уровень гемоглобина в первом триместре был значительно ниже. После поправки на возможные факторы, влияющие на факторы, уровни Hb в течение первого триместра были значимо и положительно связаны с риском GDM и PE, а также были значимо и отрицательно связаны с риском преждевременных родов. Более того, среди женщин, у которых ИМТ до беременности был <24 кг / м ( 2 ), уровни гемоглобина выше 130 г / л в течение первого триместра были связаны со значительно более высоким риском ГСД и более низкими показателями преждевременных родов.Кроме того, когда уровень гемоглобина превышал 150 г / л, риск ПЭ был значительно повышен. Однако среди женщин, у которых ИМТ до беременности был ≥24 кг / м 2 , только уровни Hb выше 150 г / л повышали риск ГСД.
Подобно нашим результатам, более раннее обсервационное исследование 730 китайских беременных женщин показало, что высокие уровни гемоглобина у матери (> 130 г / л) в первом триместре были связаны со значительно более высокой частотой ГСД [16]. Еще в 1986 году Мерфи и др.[17] провели исследование с участием 44 316 беременных женщин и обнаружили, что у женщин с высоким уровнем гемоглобина до 24 недель беременности частота ПЭ была значительно выше. Недавнее ретроспективное когортное исследование 920 одноплодных беременностей показало, что у беременных женщин со значением Hb ≥125 г / л до 14 недель гестации риск развития ПЭ и ГСД повышен в 3,8 и 3,3 раза соответственно по сравнению с женщинами со значениями гемоглобина более 110–124 г / л [10]. Аналогичным образом, в отчете Мехрабиана и Хоссейни [18] о 973 беременностях в период 2011–2012 гг. Значительно более высокая частота ГСД и ПЭ была обнаружена среди женщин, у которых на ранних сроках беременности уровень гемоглобина ≥125 г / л, чем у женщин со значениями гемоглобина <125 г. / L.Значения OR относительных рисков составили 3,7 (95% ДИ; от 2,2 до 6,4) и 5,4 (95% ДИ; от 2,8 до 10,5) соответственно [18]. Наши результаты в целом соответствуют результатам этих исследований. Беременные женщины в нашем исследовании с уровнем гемоглобина ≥130 г / л имели повышенный риск ГСД и ПЭ, и связь становилась более значительной, когда уровень гемоглобина превышал 150 г / л.
Связь, наблюдаемая в этом и других исследованиях между уровнями Hb и риском GDM и PE, кажется биологически правдоподобной. Примечательно, что результаты, представленные как в нашем, так и в других исследованиях [12, 16], показали, что женщины с высоким уровнем гемоглобина имели более высокий ИМТ до беременности, что позволяет предположить, что высокий уровень гемоглобина может быть следствием их лучшего статуса питания.Кроме того, высокий статус питания может быть связан с повышенным риском ГСД и ПЭ. Кроме того, мы предположили, что высокий уровень гемоглобина может отражать перегрузку железом, поскольку было подтверждено, что добавление железа в высоких дозах играет роль в возникновении ГСД [19]. Накапливающиеся данные продемонстрировали, что железо является сильным прооксидантом, а перегрузка железом может усиливать окислительный стресс β-клеток, вызывая резистентность к инсулину и нарушая метаболизм глюкозы [20].
Механизм, лежащий в основе вклада Hb в PE, может в первую очередь включать высокую вязкость крови.Гипервязкость может напрямую снижать кровоток в микрососудах с низкой кинетической силой, таких как плацента [21]. Это может привести к снижению перфузии и оксигенации ткани плаценты, что усугубляет гипоксию ткани плаценты как прямой результат низкой скорости плацентарного кровообращения и снижения поступления кислорода. Более того, Hb играет непосредственную роль в регуляции оксида азота (NO) и функции эндотелия. NO является сильнодействующим вазодилататором и может расслаблять гладкомышечные клетки сосудов. Свободный гемоглобин может связывать и неактивный NO, что приводит к сужению сосудов с последующей гипертензией [22] и ишемией плаценты.Более того, окисленный гемоглобин может создавать гемовые отложения, полученные из метгемоглобина, на эндотелии сосудов, что, в свою очередь, напрямую повреждает эндотелий или способствует образованию атеромы за счет эффекта окисленных липопротеинов низкой плотности [23].
В дополнение к GDM и PE, наше исследование выявило значительную связь между анемией и высоким риском преждевременных родов. Кроме того, риск преждевременных родов снижался с увеличением уровня гемоглобина в первом триместре, особенно среди женщин, у которых до беременности ИМТ был <24 кг / м 2 .Другие исследования также подтвердили, что анемия является независимым фактором риска преждевременных родов, хотя исследования уровней гемоглобина и риска преждевременных родов немногочисленны. Ретроспективное исследование, сравнивающее одноплодную беременность с анемией и без нее в течение первого триместра у женщин, родивших в период с 1988 по 2002 год, показало, что по сравнению с неанемическими женщинами более высокие показатели преждевременных родов (<37 недель беременности) были обнаружены среди женщин с анемией (10,7 % против 9,0% соответственно p <0.001). Более того, материнская анемия была независимым фактором риска преждевременных родов даже после поправки на вмешивающиеся факторы (OR = 1,2; 95% CI 1,1–1,2, p <0,001) [24]. В другой период измерения гемоглобина анализ 295 651 беременной женщины показал, что высокая частота преждевременных родов наблюдалась при уровне гемоглобина <110 г / л, а относительный риск увеличивался при уменьшении диапазона значений гемоглобина. Кроме того, женщины с уровнем гемоглобина выше 145 г / л также были связаны со значительно повышенным риском преждевременных родов (OR: 1.14; 95% ДИ 1,05, 1,25) [25]. В отличие от приведенных выше результатов, у женщин с уровнем гемоглобина> 130 г / л в нашем исследовании был значительно снижен риск преждевременных родов, а относительный риск снижался при увеличении диапазона значений гемоглобина. Однако международное многоцентровое перекрестное исследование 5690 одноплодных и первородящих беременностей показало, что не было статистически значимого влияния анемии на риск преждевременных родов [26]. По нашему мнению, различия в популяционных характеристиках исследуемых участников различных исследований могут быть основной причиной, объясняющей эти противоречивые результаты.
Кроме того, несколько исследований подтвердили, что железодефицитная анемия, а не анемия, вызванная другими причинами, влияет на преждевременные роды [27, 28]. Таким образом, они предположили, что дефицит железа может быть причиной преждевременных родов. Однако на сегодняшний день точные механизмы, лежащие в основе железодефицитной или железодефицитной анемии и преждевременных родов, еще не установлены. Возможный механизм может включать недостаточный перенос кислорода к матке, плаценте и плоду из-за нарушения транспортной способности гемоглобина, вызванного дефицитом железа.
После того, как мы провели анализ подгрупп, стратифицированных по ИМТ до беременности, мы обнаружили, что связь повышенного гемоглобина с риском развития ГСД сохраняется в каждой подгруппе. Хотя тенденция к увеличению заболеваемости ПЭ с повышенным уровнем гемоглобина была отмечена только у женщин, у которых до беременности ИМТ был ≥24 кг / м 2 , защитные эффекты высоких уровней гемоглобина на преждевременные роды наблюдались только у женщин, у которых преждевременные роды были ИМТ беременности был <24 кг / м 2 . Эти результаты, по-видимому, предполагают, что уровни гемоглобина в первом триместре по-разному влияют на возникновение ПЭ и преждевременных родов в разных категориях ИМТ до беременности.Кроме того, уровни гемоглобина в первом триместре были значительно выше у женщин, у которых до беременности ИМТ был ≥24 кг / м 2 по сравнению с женщинами, у которых до беременности ИМТ был <24 кг / м 2 , и их Расчетные значения уровня гемоглобина риска в первом триместре были 150 г / л и 130 г / л соответственно. Таким образом, эти данные предполагают, что ИМТ до беременности следует учитывать при оценке уровня гемоглобина в первом триместре. Однако на сегодняшний день не существует единых стандартов, определяющих высокий уровень гемоглобина.
Наше исследование было многоцентровым и первым выполнило совместный анализ ИМТ и гемоглобина у матери до беременности на частоту ГСД, ТЭЛА и преждевременных родов. Размер выборки в нашем исследовании очень большой. Кроме того, наше исследование было проведено обученным персоналом, и большая часть данных была собрана из медицинских записей, что обеспечило стандартизацию сбора данных. Кроме того, анализ подгрупп, стратифицированный по ИМТ до беременности, позволил нам показать, что ИМТ до беременности играет роль в влиянии на взаимосвязь между уровнями гемоглобина и исходами беременности.Однако наше исследование является ретроспективным, и набранные беременные женщины были из трех городов Китая. Кроме того, есть некоторые различия между исходной когортой и последней когортой исследования. Таким образом, эти ограничения могут внести систематическую ошибку и ограничить распространение результатов исследования на всех беременных женщин в Китае. Кроме того, следует отметить, что размер выборки нашего исследования все еще может быть недостаточным в некоторых подгруппах, таких как группа женщин, у которых уровень гемоглобина был <110 г / л, а ИМТ до беременности был ≥24 кг / м 2 , что может частично объяснить несущественные результаты.Кроме того, количество участников с ПЭ и преждевременными родами также может быть недостаточным в нашем исследовании для оценки статистически значимой разницы из-за наших критериев исключения. Недавние исследования показали, что повышенные запасы железа могут играть роль в развитии GDM во время беременности [19, 29]. Тем не менее, в этом исследовании у нас нет данных относительно материнского уровня железа или ферритина, а также нет данных о приеме добавок, таких как фолиевая кислота или таблетки железа в первом триместре.Таким образом, мы не смогли ни определить, связана ли наблюдаемая анемия с дефицитом железа, ни подробно обсудить влияние добавок на анемию, ни даже провести совместный анализ уровней гемоглобина и статуса железа в настоящем исследовании. Кроме того, в зависимости от результатов нашего и других исследований, установление баланса между статусом железа и уровнями гемоглобина может стать проблемой в будущем и должно быть выявлено с помощью более тщательно разработанных исследований.
Гемоглобин A1c — ознакомьтесь с тестом
Источники, использованные в текущем обзоре
2018 обзор завершила Алина Г.Софронеску, PhD, NRCC-CC, FACB.
Стандарты лечения Американской диабетической ассоциации, 2018 г. (январь 2018 г.). Доступно на сайте https://diabetesed.net/wp-content/uploads/2017/12/2018-ADA-Standards-of-Care.pdf. По состоянию на июнь 2018 г.
(апрель 2018 г.) Национальный институт диабета, болезней органов пищеварения и почек. Тест A1C и диабет. Доступно в Интернете по адресу https://www.niddk.nih.gov/health-information/diabetes/overview/tests-diagnosis/a1c-test. По состоянию на июнь 2018 г.
Sacks D, et.al. Уточняющее измерение гемоглобина A1c. Клиническая химия сен 2017, 63 (9) 1433-1435.
Источники, использованные в предыдущих обзорах
2015 Рецензент: Ирен Шу, доктор философии, DABCC, помощник директора лаборатории, USDTL.
Американская диабетическая ассоциация (2015). Стандарты медицинской помощи при диабете. Diabetes Care , Volume 38, Supplement 1. Доступно в Интернете по адресу http://professional.diabetes.org/admin/UserFiles/0%20-%20Sean/Documents/January%20Supplement%20Combined_Final.pdf. Проверено 11.08.2015.
Diabetes.co.uk. Симптомы диабета: 3 главных признака. Доступно в Интернете по адресу http://www.diabetes.co.uk/The-big-three-diabetes-signs-and-symptoms.html. Проверено 11.08.2015.
(10 августа 2015 г.) Управление по контролю за продуктами и лекарствами США IVD OTC-Over the Counter Database. Доступно в Интернете по адресу http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfIVD/Search.cfm. Проверено 11.08.2015.
Национальная программа стандартизации гликогемоглобина, NGSP. Преобразование между NGSP, IFCC и eAG.Доступно в Интернете по адресу http://www.ngsp.org/convert1.asp. Проверено 11.08.2015.
(Обновлено в мае 2015 г.) Национальная программа стандартизации гликогемоглобина. Факторы, влияющие на результаты теста HbA1c. Доступно в Интернете по адресу http://www.ngsp.org/factors.asp. Проверено 11.08.2015.
Томас, Клейтон Л., редактор (1997). Циклопедический медицинский словарь Табера. Компания F.A. Davis, Филадельфия, Пенсильвания [18-е издание].
Пагана, Кэтлин Д. и Пагана, Тимоти Дж. (2001). Справочник Мосби по диагностическим и лабораторным испытаниям, 5-е издание: Mosby, Inc., Сент-Луис, Миссури.
(1 мая 2002 г., обновлено). Другие тесты для лечения диабета, гликозилированный гемоглобин. Информация о диабете, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США [он-лайн информация]. Доступно в Интернете по адресу http://www.fda.gov/diabetes/gluosis.html#18.
(1995-2004). Сахарный диабет. Руководство по медицинской информации Merck — Second Home Edition [Электронная информация]. Доступно в Интернете по адресу http://www.merck.com/mmhe/sec13/ch265/ch265a.html?qt=Diabetes&alt=sh.
Мбанья, Дж.et. al. Члены Рабочей группы (20 января 2004 г.). Отчет рабочей группы ADA / EASD / IDF по анализу HbA1c. Все новости EASD [Он-лайн отчет]. Доступно на сайте http://www.easd.org/. (Щелкните «Все новости» и «2004/05»).
A.D.A.M., обновлено (10 октября 2003 г., обновлено). HbA1c. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003640.htm.
(июнь 2004 г.). 2004 г. Заседание клинического консультативного комитета NGSP. 64-я ежегодная научная сессия Американской диабетической ассоциации, июнь 2004 г.NGSP, Что нового [Он-лайн информация]. Доступно в Интернете по адресу http://www.missouri.edu/~diabetes/ngsp/indexwn.html.
Пагана, Кэтлин Д. и Пагана, Тимоти Дж. (© 2007). Справочник Мосби по диагностике и лабораторным испытаниям, 8-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 503-505.
Литтл Р., Натан Д. и Сакс Д. (9 декабря 2008 г.). Гемоглобин A1c: новые применения сегодня и возможности в будущем. AACC [Аудиоконференция].
Холт, Э. (17 июня 2008 г., обновлено). HbA1c.Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003640.htm. Доступ 13.12.08.
Американская диабетическая ассоциация. Тест A1C. [Он-лайн информация]. Доступно в Интернете по адресу http://www.diabetes.org/type-1-diabetes/a1c-test.jsp. Доступ 13.12.08.
(2008). Но что на самом деле означает мой уровень A1C? Американская диабетическая ассоциация [Он-лайн информация]. Доступно в Интернете по адресу http://www.diabetes.org//diabetes-research/summaries/nathan-what-a1c-level-means.jsp. Доступ 13.12.08.
Натан, Д. и др. al. (7 июня 2008 г.). Перевод анализа A1C в расчетные средние значения глюкозы. Уход за диабетом 31: 1473-1478, 2008 DOI: 10.2337 / dc08-0545 [Электронный журнал]. Доступно в Интернете по адресу http://care.diabetesjournals.org/cgi/content/abstract/31/8/1473. Доступ 14.12.08.
Crandall, J. (май 2007 г., редакция). Сахарный диабет. Пособие Merck для специалистов здравоохранения [Он-лайн информация]. Доступно в Интернете по адресу http: //www.merck.com / mmpe / sec12 / ch258 / ch258b.html? qt = diab & alt = sh # sec12-ch258-ch258b-1159. Доступ 14.12.08.
Комитет по консенсусу (сентябрь 2007 г.). Заявление о консенсусе по всемирной стандартизации измерения гемоглобина A1c. Уход за диабетом v30 (9). [Он-лайн журнал]. PDF-файл доступен для загрузки по адресу http://www.ifcc.org/4dc9925consensus.pdf.
Кан Р. и Фонсека В. (август 2008 г.). Перевод теста A1c. DiabetesCare v 31 (8) [Он-лайн информация].PDF-файл доступен для загрузки по адресу http://professional.diabetes.org/Content/Editorial.pdf. Доступ 14.12.08.
(ноябрь 2007 г.). Серповидно-клеточная характеристика и другие гемоглобинопатии и диабет: важная информация для врачей. Национальный центр обмена информацией по диабету [Он-лайн информация]. Доступно в Интернете по адресу http://diabetes.niddk.nih.gov/dm/pubs/hemovari-A1C/index.htm. Доступ 14.12.08.
S11 (2008 г.). Вопросы и ответы Расчетное среднее значение глюкозы: альтернатива A1C. Американская диабетическая ассоциация [Он-лайн информация].Доступно в Интернете по адресу http://professional.diabetes.org/GluosisCalculator.aspx. Доступ 21.12.08.
Американская диабетическая ассоциация. Краткое содержание: Стандарты медицинской помощи при диабете — 2010. Январь 2010 г. Уход за диабетом 33: S4-S10.
(январь 2010 г.) Заявление эндокринного общества об использовании A1c для диагностики диабета и оценки риска. PDF-файл доступен для загрузки по адресу http://www.endo-society.org/advocacy/upload/TES-Statement-on-A1C-Use.pdf. По состоянию на январь 2010 г.
(обновлено 19 июня 2012 г.). Тест A1C и диабет. Национальный институт диабета, болезней органов пищеварения и почек (NIDDK) [онлайн-информация]. Доступно в Интернете по адресу http://diabetes.niddk.nih.gov/dm/pubs/A1CTest/. По состоянию на октябрь 2012 г.
Топивала, С. (Обновлено 29 апреля 2012 г.). HbA1c. Медицинская энциклопедия MedlinePlus [Он-лайн информация]. Доступно в Интернете по адресу http://www.nlm.nih.gov/medlineplus/ency/article/003640.htm. По состоянию на октябрь 2012 г.
Горовиц, Г. (Обновлено 6 января 2012 г.).Тестирование гемоглобина A1c. Справочник по Medscape [Он-лайн информация]. Доступно в Интернете по адресу http://emedicine.medscape.com/article/2049478-overview#showall. По состоянию на октябрь 2012 г.
(© 1995-2012). A1C. Американская диабетическая ассоциация [Он-лайн информация]. Доступно в Интернете по адресу http://www.diabetes.org/living-with-diabetes/treatment-and-care/blood-gluosis-control/a1c/. По состоянию на октябрь 2012 г.
(© 1995-2012). Гемоглобин A1c, кровь. Клиника Мэйо Медицинские лаборатории Мэйо [Он-лайн информация].Доступно в Интернете по адресу http://www.mayomedicallaboratories.com/test-catalog/Overview/82080. По состоянию на октябрь 2012 г.
(Обновлено 4 ноября 2011 г.). Для людей с африканским, средиземноморским или юго-восточным азиатским наследием: важная информация о анализах крови на диабет. Национальный институт диабета, болезней органов пищеварения и почек (NIDDK) [онлайн-информация]. Доступно в Интернете по адресу http://diabetes.niddk.nih.gov/dm/pubs/traitA1C/index.aspx. По состоянию на октябрь 2012 г.
Пагана, К. Д. и Пагана, Т.J. (© 2011). Справочник Мосби по диагностическим и лабораторным испытаниям, 10-е издание: Mosby, Inc., Сент-Луис, Миссури. С. 508-510.
Inzucchi, S. et. al. (19 апреля 2012 г., онлайн). Управление гипергликемией при диабете 2 типа: подход, ориентированный на пациента, Заявление о позиции Американской диабетической ассоциации (ADA) и Европейской ассоциации по изучению диабета (EASD). Уход за диабетом 2012; 35: 1364–1379. [Он-лайн информация]. PDF-файл доступен для загрузки на сайте http: //care.diabetesjournals.org / content / early / 2012/04/19 / dc12-0413.full.pdf. По состоянию на октябрь 2012 г.
Заявление о консенсусе 2010 г. по всемирной стандартизации измерения гемоглобина A1c. Рагнар Ханас и Гарри Джон от имени Международного комитета по консенсусу HbA1c. Опубликовано 27 мая 2010 г. Последняя версия доступна в Интернете по адресу http://www.clinchem.org/cgi/doi/10.1373/clinchem.2010.150540. По состоянию на октябрь 2012 г.
Проблема «ломкого» диабета. Предупреждение о состоянии здоровья Джонса Хопкинса. Доступно в Интернете по адресу http: // www.johnshopkinshealthalerts.com/alerts/diabetes/JohnsHopkinsDiabetesAlert_3541-1.html. По состоянию на октябрь 2012 г.
(2013 ©) Американская диабетическая ассоциация. Основы диабета, диагностика диабета и преддиабета. Доступно в Интернете по адресу http://www.diabetes.org/diabetes-basics/diagnosis/?loc=DropDownDB-diagnosis. По состоянию на май 2012 г.
Железодефицитная анемия — Диагностика и лечение
Диагноз
Чтобы диагностировать железодефицитную анемию, ваш врач может провести тесты, чтобы найти:
- Размер и цвет эритроцитов. При железодефицитной анемии эритроциты меньше и бледнее по цвету, чем обычно.
- Гематокрит. Это процент объема вашей крови, состоящий из красных кровяных телец. Нормальные уровни обычно составляют от 35,5 до 44,9 процента для взрослых женщин и от 38,3 до 48,6 процента для взрослых мужчин. Эти значения могут меняться в зависимости от вашего возраста.
- Гемоглобин. Уровень гемоглобина ниже нормы указывает на анемию. Нормальный диапазон гемоглобина обычно определяется как 13.От 2 до 16,6 граммов (г) гемоглобина на децилитр (дл) крови для мужчин и от 11,6 до 15 г / дл для женщин.
- Ферритин. Этот белок помогает накапливать железо в организме, а низкий уровень ферритина обычно указывает на низкий уровень накопленного железа.
Дополнительные диагностические тесты
Если анализ крови указывает на железодефицитную анемию, ваш врач может назначить дополнительные тесты для определения основной причины, например:
- Эндоскопия. Врачи часто проверяют кровотечение из грыжи пищеводного отверстия диафрагмы, язвы или желудка с помощью эндоскопии. В этой процедуре тонкая трубка с подсветкой, оснащенная видеокамерой, проходит через горло в желудок. Это позволяет вашему врачу осмотреть трубку, идущую от вашего рта к вашему желудку (пищеводу) и вашему желудку, чтобы найти источники кровотечения.
- Колоноскопия. Чтобы исключить источники кровотечения из нижних отделов кишечника, врач может порекомендовать процедуру, называемую колоноскопией.Тонкая гибкая трубка с видеокамерой вводится в прямую кишку и направляется к толстой кишке. Обычно во время этого теста вам вводят седативные препараты. Колоноскопия позволяет вашему врачу осмотреть часть или всю вашу толстую и прямую кишку, чтобы найти внутреннее кровотечение.
- Ультразвук. Женщинам также может пройти УЗИ органов малого таза для поиска причины обильного менструального кровотечения, например миомы матки.
Ваш врач может назначить те или иные анализы после пробного периода лечения препаратами железа.
Дополнительная информация
Показать дополнительную информацию
Лечение
Для лечения железодефицитной анемии врач может порекомендовать вам принимать добавки железа. При необходимости врач также поможет устранить первопричину дефицита железа.
Железные добавки
Ваш врач может порекомендовать отпускаемые без рецепта железные таблетки для пополнения запасов железа в вашем организме. Ваш врач сообщит вам правильную дозу.Железо также доступно в жидкой форме для младенцев и детей. Чтобы повысить вероятность того, что ваше тело поглотит железо, содержащееся в таблетках, вам могут быть даны инструкции:
- Железные таблетки принимать натощак. Если возможно, принимайте железные таблетки на пустой желудок. Однако, поскольку таблетки железа могут вызвать расстройство желудка, вам может потребоваться принимать таблетки железа во время еды.
- Не принимайте железо с антацидами. Лекарства, которые немедленно снимают симптомы изжоги, могут нарушать всасывание железа.Принимайте железо за два часа до или через четыре часа после приема антацидов.
- Принимайте таблетки железа с витамином С. Витамин С улучшает усвоение железа. Ваш врач может порекомендовать принимать таблетки железа со стаканом апельсинового сока или с добавкой витамина С.
Добавки железа могут вызвать запор, поэтому ваш врач может также порекомендовать смягчители стула. Железо может сделать стул черным, что является безвредным побочным эффектом.
Дефицит железа нельзя исправить в одночасье.Возможно, вам придется принимать добавки железа в течение нескольких месяцев или дольше, чтобы восполнить запасы железа. Как правило, вы начнете чувствовать себя лучше примерно через неделю лечения. Спросите своего врача, когда нужно повторно проверять кровь для измерения уровня железа. Чтобы быть уверенным, что ваши запасы железа восполнены, вам может потребоваться принимать добавки железа в течение года или более.
Лечение основных причин дефицита железа
Если добавки железа не повышают уровень железа в крови, вероятно, причиной анемии является источник кровотечения или проблема с усвоением железа, которую врач должен исследовать и лечить.В зависимости от причины, лечение железодефицитной анемии может включать:
- Лекарства, такие как оральные контрацептивы для облегчения обильных менструальных выделений
- Антибиотики и другие препараты для лечения язвенной болезни
- Операция по удалению кровоточащего полипа, опухоли или миомы
При тяжелой степени железодефицитной анемии может потребоваться внутривенное введение железа или переливание крови, чтобы быстро восполнить железо и гемоглобин.
Подготовка к приему
Запишитесь на прием к врачу, если у вас есть какие-либо признаки и симптомы, которые вас беспокоят.Если у вас диагностирована железодефицитная анемия, вам могут потребоваться тесты для поиска источника кровопотери, в том числе тесты для исследования желудочно-кишечного тракта.
Вот некоторая информация, которая поможет вам подготовиться к приему и чего ожидать от врача.
Что вы можете сделать
- Запишите все симптомы, которые вы испытываете, включая те, которые могут показаться не связанными с причиной, по которой вы записались на прием.
- Запишите ключевую личную информацию, включая любые серьезные стрессы или недавние изменения в жизни.
- Составьте список всех лекарств, витаминов или добавок, которые вы принимаете.
- Запишите вопросы, которые можно задать своему врачу.
Ваше время с врачом ограничено, поэтому подготовка списка вопросов поможет вам максимально эффективно проводить время вместе. При железодефицитной анемии врачу следует задать несколько основных вопросов:
- Какая наиболее вероятная причина моих симптомов?
- Есть ли другие возможные причины моих симптомов?
- Является ли мое состояние временным или продолжительным?
- Какое лечение вы рекомендуете?
- Есть ли альтернативы основному подходу, который вы предлагаете?
- У меня другое заболевание.Как мне вместе лучше всего справиться с этими условиями?
- Есть ли какие-либо диетические ограничения, которым я должен следовать?
- Есть ли какие-нибудь брошюры или другие печатные материалы, которые я могу взять с собой? Какие сайты вы рекомендуете?
В дополнение к вопросам, которые вы подготовили задать своему врачу, не стесняйтесь задавать вопросы во время приема.
Чего ожидать от врача
Ваш врач, скорее всего, задаст вам ряд вопросов.Если вы будете готовы ответить на них, у вас останется время, чтобы обсудить те моменты, на которые вы хотите потратить больше времени. Ваш врач может спросить:
- Когда у вас появились симптомы?
- Насколько серьезны ваши симптомы?
- Кажется, что-нибудь улучшает ваши симптомы?
- Что может ухудшить ваши симптомы?
- Заметили ли вы необычное кровотечение, такое как обильные месячные, кровотечение из геморроя или носовое кровотечение?
- Вы вегетарианец?
- Сдавали ли вы в последнее время кровь более одного раза?
Октябрь18, 2019
Гликогемоглобин (HbA1c, A1c) | Мичиган Медицина
Обзор
Тест на гликогемоглобин или гемоглобин A1c — это анализ крови, который проверяет количество сахара (глюкозы), связанного с гемоглобином в красных кровяных тельцах. Люди, страдающие диабетом или другими состояниями, повышающими уровень глюкозы в крови, имеют больше гликогемоглобина (сахара, связанного с гемоглобином), чем обычно.
Тест A1c может использоваться для диагностики преддиабета или диабета.Тест A1c проверяет долгосрочный контроль уровня глюкозы в крови у людей с диабетом. Большинство врачей считают, что проверка уровня A1c — лучший способ проверить, насколько хорошо человек контролирует свой диабет. Этот тест можно сделать с взятием крови из вены. Иногда тест на A1c можно сделать с кровью из пальца.
Домашний тест на глюкозу крови измеряет уровень глюкозы в крови только в этот момент. Уровень глюкозы в крови меняется в течение дня по многим причинам, включая лекарства, диету, физические упражнения и уровень инсулина в крови.
Людям, страдающим диабетом, полезно иметь информацию о долгосрочном контроле уровня сахара в крови. Результат теста A1c не меняется при недавних изменениях в диете, физических упражнениях или лекарствах.
Глюкоза стабильно связывается с гемоглобином в красных кровяных тельцах. Поскольку эритроциты живут от 3 до 4 месяцев, тест A1c показывает, сколько глюкозы содержится в плазменной части крови. Этот тест показывает, насколько хорошо ваш диабет контролировался за последние 2-3 месяца и нужно ли менять план лечения диабета.
Тест A1c также может помочь вашему врачу определить, насколько велик ваш риск развития проблем, связанных с диабетом, таких как почечная недостаточность, проблемы со зрением и онемение ног или ступней. Сохранение уровня A1c в целевом диапазоне может снизить вероятность возникновения проблем.
Почему это делается
Этот тест проводится для:
- Диагностика преддиабета и диабета.
- Проверьте свое лечение от диабета.
Как подготовить
Вам не нужно прекращать есть до того, как вы пройдете тест A1c.Этот тест можно проводить в любое время дня, даже после еды.
Как это делается
Медицинский работник, взявший образец вашей крови:
- Обернет эластичную ленту вокруг вашего плеча, чтобы остановить кровоток. Это увеличивает размер вены под лентой, что упрощает введение иглы в вену.
- Очистите место для иглы спиртом.
- Введите иглу в вену. Может потребоваться более одной иглы.
- Присоедините к игле трубку, чтобы наполнить ее кровью.
- Снимите повязку с руки, когда наберется достаточно крови.
- Поместите марлевую салфетку или ватный диск на место иглы, когда игла будет удалена.
- Надавите на участок, а затем наложите повязку.
Как это чувствуется
Образец крови берется из вены на руке. Плечо оборачивается резинкой. Может ощущаться стеснение.Вы можете вообще ничего не чувствовать от иглы или можете почувствовать быстрое укусывание или защемление.
Риски
Анализ крови
Очень мала вероятность возникновения проблемы из-за взятия пробы крови из вены.
- На этом участке может образоваться небольшой синяк. Вы можете снизить вероятность образования синяков, если надавите на это место в течение нескольких минут.
- В редких случаях после взятия пробы крови вена может опухнуть. Эта проблема называется флебитом.Для лечения этого состояния можно использовать теплый компресс несколько раз в день.
Результаты
A1c — это анализ крови, который проверяет количество сахара (глюкозы), связанного с гемоглобином. Результат отображается в процентах. Результат вашего теста A1c также можно использовать для оценки вашего среднего уровня сахара в крови. Это называется вашим расчетным средним уровнем глюкозы или eAG. Ваш врач сообщит вам результаты анализов через несколько дней.
Критерии диагностики диабета Американской диабетической ассоциации (ADA) включают возможность тестирования A1c.Ваш врач может повторить тест, чтобы подтвердить диагноз диабета.
Нормальный
В каждой лаборатории свой диапазон нормального значения. В вашем лабораторном отчете должен быть указан диапазон, который ваша лаборатория использует для каждого теста. Нормальный диапазон — это просто ориентир. Ваш врач также рассмотрит ваши результаты в зависимости от вашего возраста, состояния здоровья и других факторов. Значение, выходящее за пределы нормального диапазона, может быть для вас нормальным.
Нормальный | Менее 5.7% | |||
Предиабет (повышенный риск диабета) | 5,7% –6,4% | |||
Диабет | 6,5% и выше 005 |
A1c% | Расчетное среднее значение глюкозы в плазме (мг / дл) | / Л) | ||
|---|---|---|---|---|
6% | 126 | 7.0 | ||
7% | 154 | 8,6 | ||
8% | 183 | 183 | 10 | 11,8 |
10% | 240 | 13,4 | ||
11% | 141499 | |||
12% | 298 | 16,5 |
Высокие значения
Некоторые медицинские условия могут повышать уровень A1c, но результаты могут оставаться в пределах нормы. Эти состояния включают синдром Кушинга, феохромоцитому и синдром поликистозных яичников (СПКЯ).
Лечение кортикостероидами повышает уровень A1c.
Что влияет на тест
Причины, по которым вы не сможете пройти тест или почему его результаты могут оказаться бесполезными, включают:
- Серьезная потеря крови или переливание крови в течение последних 3 месяцев.
- Наличие определенных заболеваний, таких как серповидноклеточная анемия, гемолитическая анемия, некоторые типы талассемии и тяжелое заболевание почек.
- Находится на гемодиализе.
- Прием лекарства на основе эритропоэтина (ESA).
- Находится во втором или третьем триместре беременности.
- Удаление селезенки. Это изменяет нормальный жизненный цикл эритроцитов и уровень A1c.
Список литературы
Цитаты
- Американская диабетическая ассоциация (2019).Стандарты медицинской помощи при сахарном диабете — 2019. Уход за диабетом , 42 (Приложение 1): S1 – S193. По состоянию на 17 декабря 2018 г.
Кредиты
Текущий по состоянию на:
31 августа 2020 г.
Автор: Healthwise Staff
Медицинский обзор:
Э. Грегори Томпсон, врач внутренних болезней
Кэтлин Ромито, доктор медицины, семейная медицина
Адам Хусни, доктор медицины, семейная медицина
Мэтью И.Ким, доктор медицины — эндокринология
Дэвид К.В. Лау, доктор медицинских наук, FRCPC — эндокринология
По состоянию на 31 августа 2020 г.
Автор:
Здоровый персонал
Медицинское обозрение: E. Грегори Томпсон, врач-терапевт и Кэтлин Ромито, доктор медицины, семейная медицина и Адам Хусни, доктор медицины, семейная медицина, и Мэтью И. Ким, доктор медицины, эндокринология и Дэвид К.W. Lau MD, PhD, FRCPC — Эндокринология
.
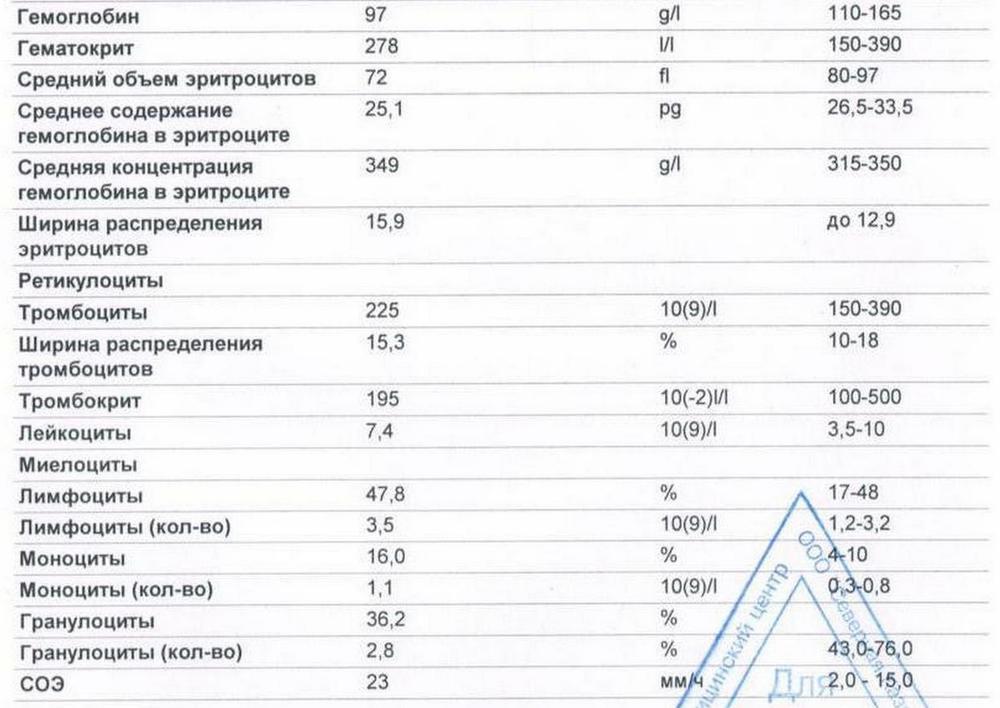 Особенно, если в организме не хватает фолиевой кислоты и витамина В12.
Особенно, если в организме не хватает фолиевой кислоты и витамина В12. Особенно это касается красных сортов рыбы, а также вяленой рыбы и морепродуктов. Поэтому любители сушеной рыбки или кальмаров должны умерить свою страсть к подобным продуктам;
Особенно это касается красных сортов рыбы, а также вяленой рыбы и морепродуктов. Поэтому любители сушеной рыбки или кальмаров должны умерить свою страсть к подобным продуктам; А продукты распада алкоголя стимулируют выработку крови. Поэтому врачи заметили, что у регулярно выпивающих людей уровень гемоглобина, как правило, повышен;
А продукты распада алкоголя стимулируют выработку крови. Поэтому врачи заметили, что у регулярно выпивающих людей уровень гемоглобина, как правило, повышен; На состав крови могут повлиять также высокая эмоциональность и слабая стрессоустойчивость.
На состав крови могут повлиять также высокая эмоциональность и слабая стрессоустойчивость.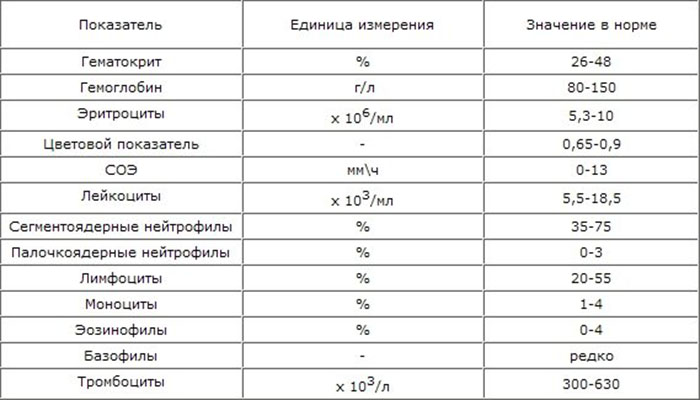 Поэтому для такого периода является нормальным снижение гемоглобина. Если месячные необильные, мажущие, это может свидетельствовать об увеличенном уровне железа и большой вязкости крови.
Поэтому для такого периода является нормальным снижение гемоглобина. Если месячные необильные, мажущие, это может свидетельствовать об увеличенном уровне железа и большой вязкости крови.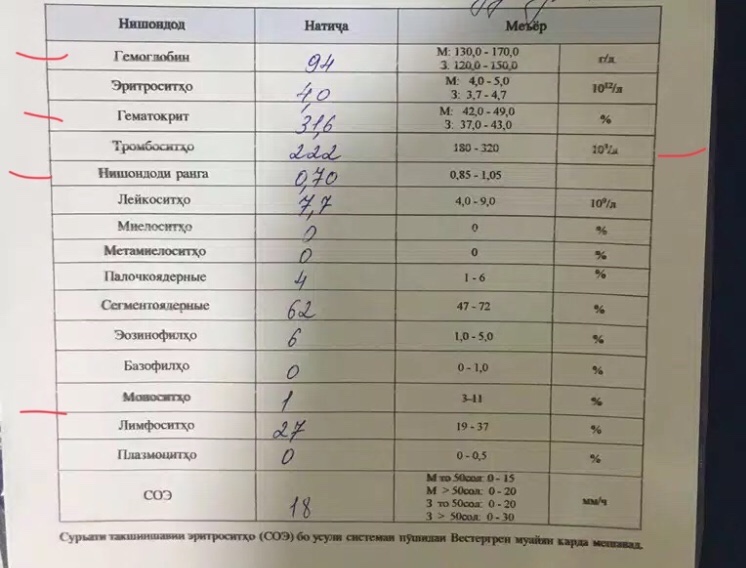
 Организм может отреагировать на это повышением гемоглобина;
Организм может отреагировать на это повышением гемоглобина;